专题08电解质【名师精讲指南篇】【高考真题再现】1.【2016年高考海南卷】向含有MgCO3固体的溶液中滴加少许浓盐酸(忽略体积变化),下列数值变小的是()A.c(CO32−)B.c(Mg2+)C.c(H+)D.Ksp(MgCO3)【答案】A2.【2016年高考江苏卷】下列图示与对应的叙述不相符合的是()A.图甲表示燃料燃烧反应的能量变化B.图乙表示酶催化反应的反应速率随反应温度的变化C.图丙表示弱电解质在水中建立电离平衡的过程D.图丁表示强碱滴定强酸的滴定曲线【答案】A3.【2016年高考江苏卷】H2C2O4为二元弱酸
20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0
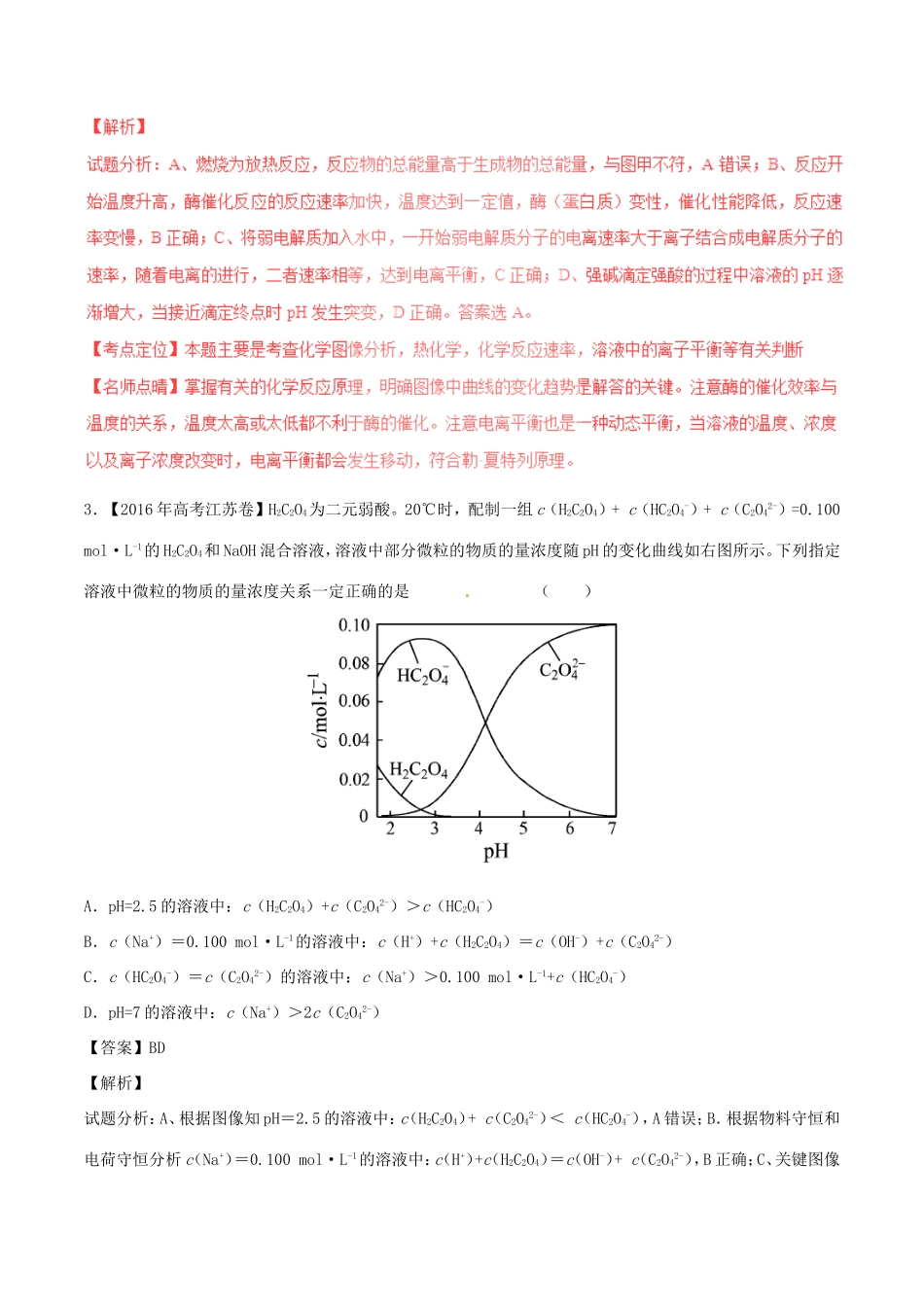
100mol·L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如右图所示
下列指定溶液中微粒的物质的量浓度关系一定正确的是()A.pH=2
5的溶液中:c(H2C2O4)+c(C2O42-)>c(HC2O4-)B.c(Na+)=0
100mol·L-1的溶液中:c(H+)+c(H2C2O4)=c(OH-)+c(C2O42-)C.c(HC2O4-)=c(C2O42-)的溶液中:c(Na+)>0
100mol·L-1+c(HC2O4-)D.pH=7的溶液中:c(Na+)>2c(C2O42-)【答案】BD【解析】试题分析:A、根据图像知pH=2
5的溶液中:c(H2C2O4)+c(C2O42-)<c(HC2O4-),A错误;B.根据物料守恒和电荷守恒分析c(Na+)=0
100mol·L-1的溶液中:c(H+)+c(H2C2O4)=c(OH-)+c(C2O42-),B正确;C、关键图像可知c(HC2O4-)=c(C2O42-)的溶液显酸性,溶液为等物质的量浓度的草酸氢钠和草酸钠的混合溶液,在溶液中:c(Na+)=0
100mol·L-1+c(HC