溶液中的三大守恒关系适用学科适用区域知识点高中化学适用年级高中三年级课标版试用地区课时时长(分钟)601
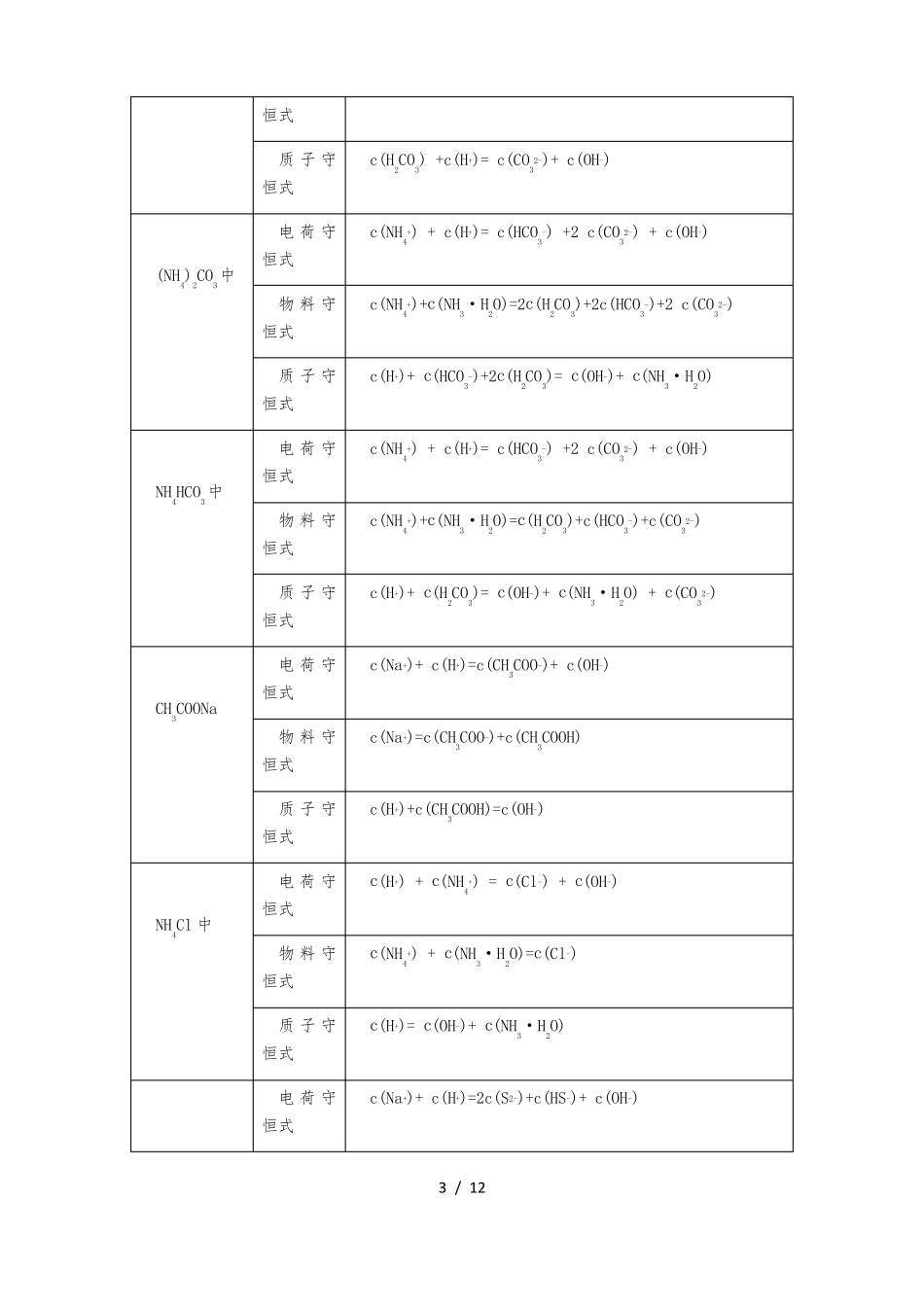
溶液中三个守恒关系的书写2
三个守恒关系的应用3
比较离子浓度大小的方法与规律4
影响水解平衡的因素教学目标知识与技能:掌握溶液中的三个守恒关系过程与方法:培养学生的观察能力、分析能力和解决实际问题的能力情感态度与价值观:体验科学探究的艰辛与愉悦,增强为人类的文明进步学习化学的责任感和使命感
教学重点教学难点溶液中三个守恒关系的书写、三个守恒关系的应用溶液中三个守恒关系的书写、三个守恒关系的应用教学过程一、复习预习复习盐类水解的相关知识,了解盐类水解的实质二、知识讲解考点1:电荷守恒电解质溶液中的阴离子的负电荷总数等于阳离子的正电荷总数例如,在NaHCO3溶液中,有如下关系:1/12C(Na)+c(H)==c(HCO3)+c(OH)+2c(CO3)考点2:物料守恒就电解质溶液而言,物料守恒是指电解质发生变化(反应或电离)前某元素的原子(或离子)的物质的量等于电解质变化后溶液中所有含该元素的原子(或离子)的物质的量之和
实质上,物料守恒属于原子个数守恒和质量守恒
例如:在Na2S溶液中存在着S的水解、HS的电离和水解、水的电离,粒子间有如下关系c(S)+c(HS)+c(H2S)==1/2c(Na)(Na,S守恒)C(HS)+2c(S)+c(H)==c(OH)(H、O原子守恒)例如:在NaHS溶液中存在着HS的水解和电离与水的电离
――2――2――++2―2――++――2―HS+H2O―H2S+OH;HS――H+S;H2O―+2―H+OH2―++―从物料守恒的角度分析,有如下等式:c(HS)+C(S)+c(H2S)==c(Na);从电荷守恒的角度分析,有如下等式:c(HS)+2(S)+c(OH)==c(Na)+c(H);将以上两式相加,有:c(S)+c(OH)==c(H2S