小结:髀(6种):HCkH2SO4、HNOjxHBr、HI、HC1O4强电强电解质完全电离,书写时用“=”号弱电解质部分电离,书时用“一”号强等注意:酸式盐电水溶液中的离子平衡考点一弱电解质的电离平衡1、电解质与非电解质(1)电解质:在水溶液中或熔融状态时能够导电的化合物(2)非电解质:在水溶液中和熔融状态都不能导电的化合物注意:(1)单质与混合物既不是电解质也不是非电解质(2)CO,NHs等溶于水得到的水溶液能导电,但它们不是电解质,因为导电不是其自身电离的离子
(3)强电解质不等于易溶于水的化合物(如BaS(\不溶于水,但溶于水的BaSO,全部电离,故BaSOi为强电解质)一一电解质的强弱与导电性、溶解性无关2
强电解质与弱电解质⑴概念(2)与化合物类型的关系强电解质主要是大部分离子化合物及少数共价化合物
弱电解质主要是共价化合物
(3)强弱电解质的区分依据不是看该物质溶解度的人小,也不是看其水溶液导电能力的强弱,而是看溶于水的部分是否完全电离
(1)电离平衡的建立在一定条件下(如温度、压强等),当弱电解质电离的速率和离子结合成分子的速率相等时,电离过程达到了平衡
(2)电离平衡的特征(3)外界条件对电离平衡的影响①内因:弱电解质本身的性质
温度:升高温度,电离平衡向电离方向移动,电离程度增人,原因是电离过程吸热
浓度:加水稀释,使弱电解质的浓度减小,电离平衡向电离的方向移动,电离程度增人
同离子效应:例如向CHsCOOH溶液中加入CHsCOONa固体,溶液中c(CH3COO")増人,CH3COOH的电离平衡向左(填“左”或石")移动,电离程度减小,c(H)减小,pH值增大
(4)电离过程是可逆过程,可直接用化学平•衡移动原理去分析电离平衡
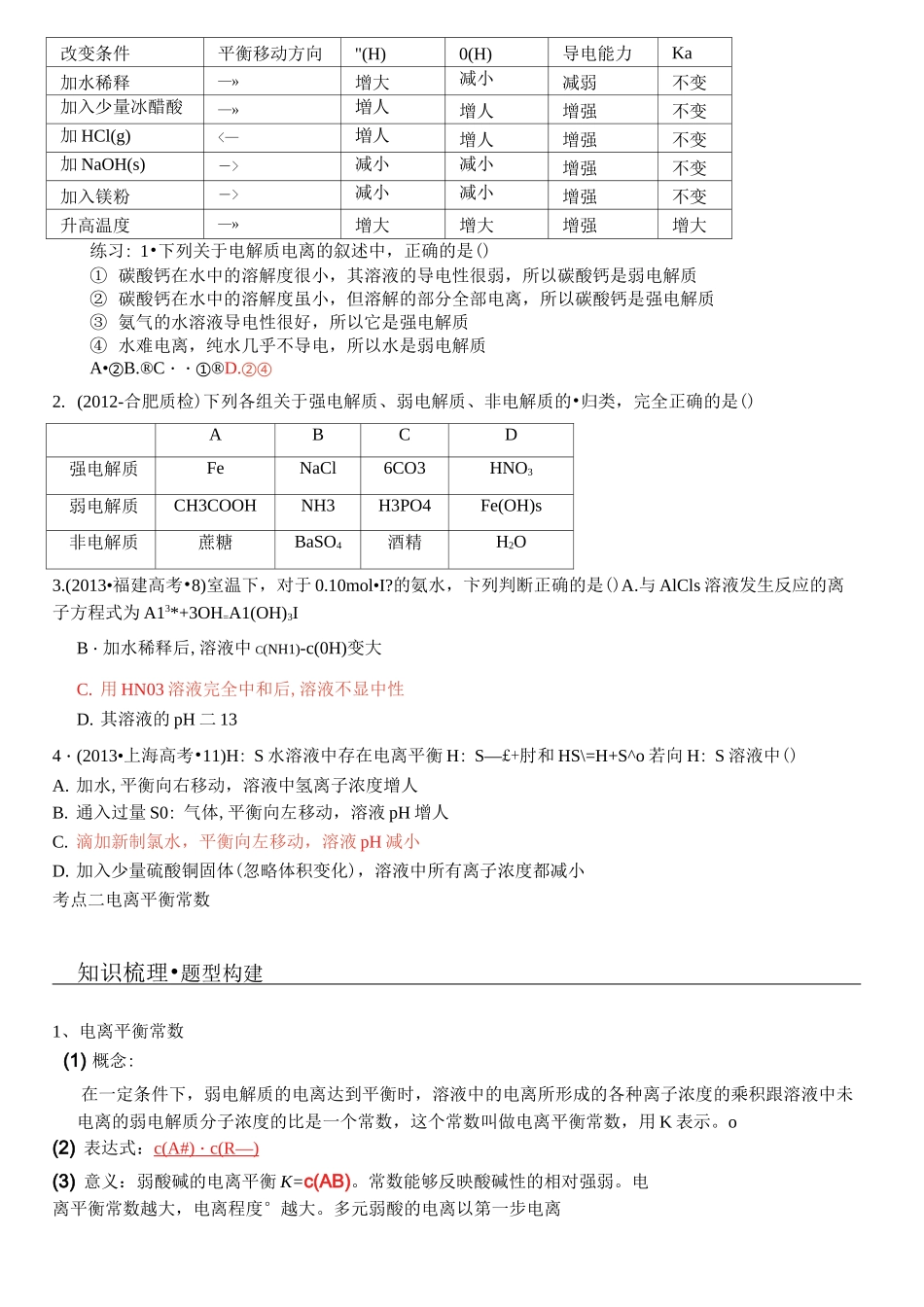
1mol-L-1CH3COOH溶液为例:CH3COOH^="CH3COO正向吸热)
实例(稀溶液)CH3