专题4××陌生反应方程式对接高考题型考查年份2021年全国甲卷、乙关联知识点非氧化还原反应陌生化学(离子)方程式、氧化还原反应陌生化学(离子)方程式的书写非氧化还原反应陌生化学(离子)工艺流程题、实验题中陌生反应方程式卷2021年新高考各省方程式、氧化还原反应陌生化学(离子)方程式的书写、电化学中陌生电极反应式的书写方法点拨信息型化学(离子、电极)方程式书写题的基本解题思路是:考法1非氧化还原反应陌生化学(离子)方程式的书写新情境下非氧化还原类化学(离子)方程式的书写,因没有涉及元素化合物的变化,故组成物质的各元素在发生反应时复分解重组,生成常见物质,一般用观察法即可配平
1.书写非氧化还原反应化学(离子)方程式的步骤:①根据实验事实写出反应物和生成物的化学式,①配平化学方程式,①注明化学方程式发生的条件并注明“↑”、“↓”
2.运用“证据→推理→符号”思路书写新情况化学(离子)方程式的基本过程如下:“读”取题目中的有效信息(证据),写出反应物和生成物的符号(推理+表征),再依据质量守恒、电荷守恒(基本规律),即可轻松写出规范的方程式
3.根据“中和”原理或“强酸制弱酸”原理书写化学(离子)方程式
4.根据“广义”的水解书写化学(离子)方程式:广义的水解观认为,无论是盐的水解还是非盐的水解,其最终结果都是参与反应的物质和水分别离解成两部分,再重新组合成新的物质
5.根据对热稳定性的理解书写化学(离子)方程式
例题1.(2021年河北卷)绿色化学在推动社会可持续发展中发挥着重要作用
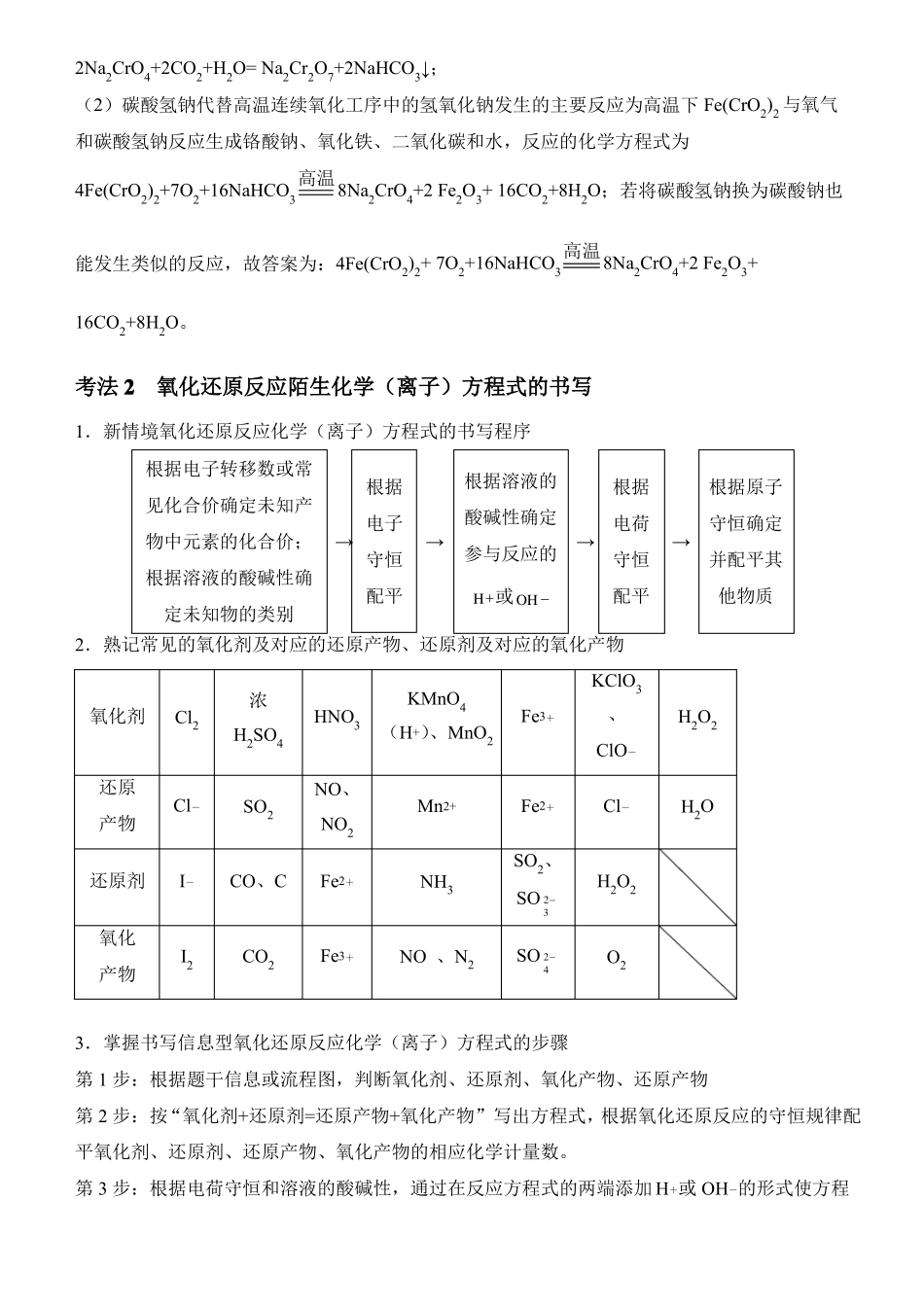
某科研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了Cr—Fe—Al—Mg的深度利用和Na+内循环
工艺流程如图:回答下列问题:(1)工序①中发生反应的离子方程式为___
(2)物质V可代替高温连续氧化工序中的NaOH,此