-1-专题40沉淀溶解平衡(满分42分时间20分钟)姓名:_______________班级:_______________得分:_______________1.已知25℃时,CaCO3饱和溶液中c(Ca2+)为5
3×10-5mol/L、MgCO3的饱和溶液中c(Mg2+)为2
6×10-3mol/L
若在5mL浓度均为0
01mol/L的CaCl2和MgCl2溶液中,逐滴加入5mL0
012mol/LNa2CO3溶液,充分反应后过滤得到溶液M和沉淀N(不考虑溶液体积的变化)
下列观点不正确的是A.25℃时,Ksp(CaCO3)=2
8×10-9B.加入Na2CO3溶液的过程中,先生成CaCO3沉淀C.滤液M中:c(Cl-)>c(Na+)>c(Mg2+)>c(CO3-)>c(OH-)D.滤液M中:【答案】D【解析】点睛:A.根据Ksp=c(Ca2+)×c(CO32-)计算;B.Ksp越小,越易生成沉淀;C.计算混合后各离子浓度,可比较大小;D.结合C的计算,溶液中没有生成碳酸镁沉淀
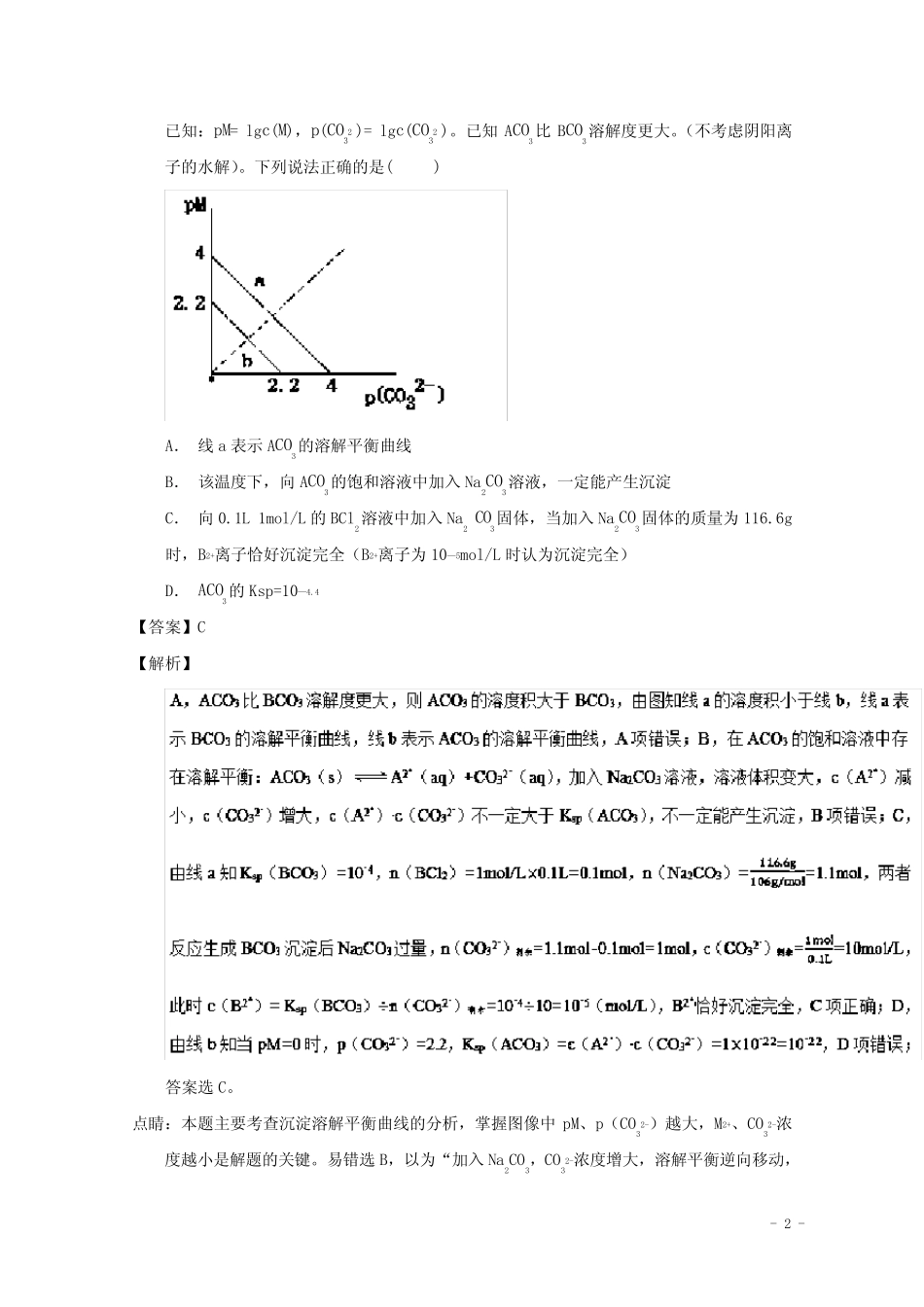
2.一定温度下,两种碳酸盐MCO3和(M分别为A和B两种离子)的沉淀溶解平衡曲线如图所示
-2-已知:pM=−lgc(M),p(CO32−)=−lgc(CO32−)
已知ACO3比BCO3溶解度更大
(不考虑阴阳离子的水解)
下列说法正确的是()A.线a表示ACO3的溶解平衡曲线B.该温度下,向ACO3的饱和溶液中加入Na2CO3溶液,一定能产生沉淀C.向0
1L1mol/L的BCl2溶液中加入Na2CO3固体,当加入Na2CO3固体的质量为116
6g时,B2+离子恰好沉淀完全(B2+离子为10—5mol/L时认为沉淀完全)D.ACO3的Ksp=10—4
4【答案】C【解析】答案选C
点睛:本题主要考查沉淀溶解平衡曲线的分析,掌握图像中pM、p(CO32-)越大,M2+、CO32-浓度越小