高中化学原电池知识练习题一、单选题1
最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程
反应过程的示意图如下:下列说法正确的是()A
CO和O生成2CO是吸热反应B
在该过程中,CO断键形成C和OC
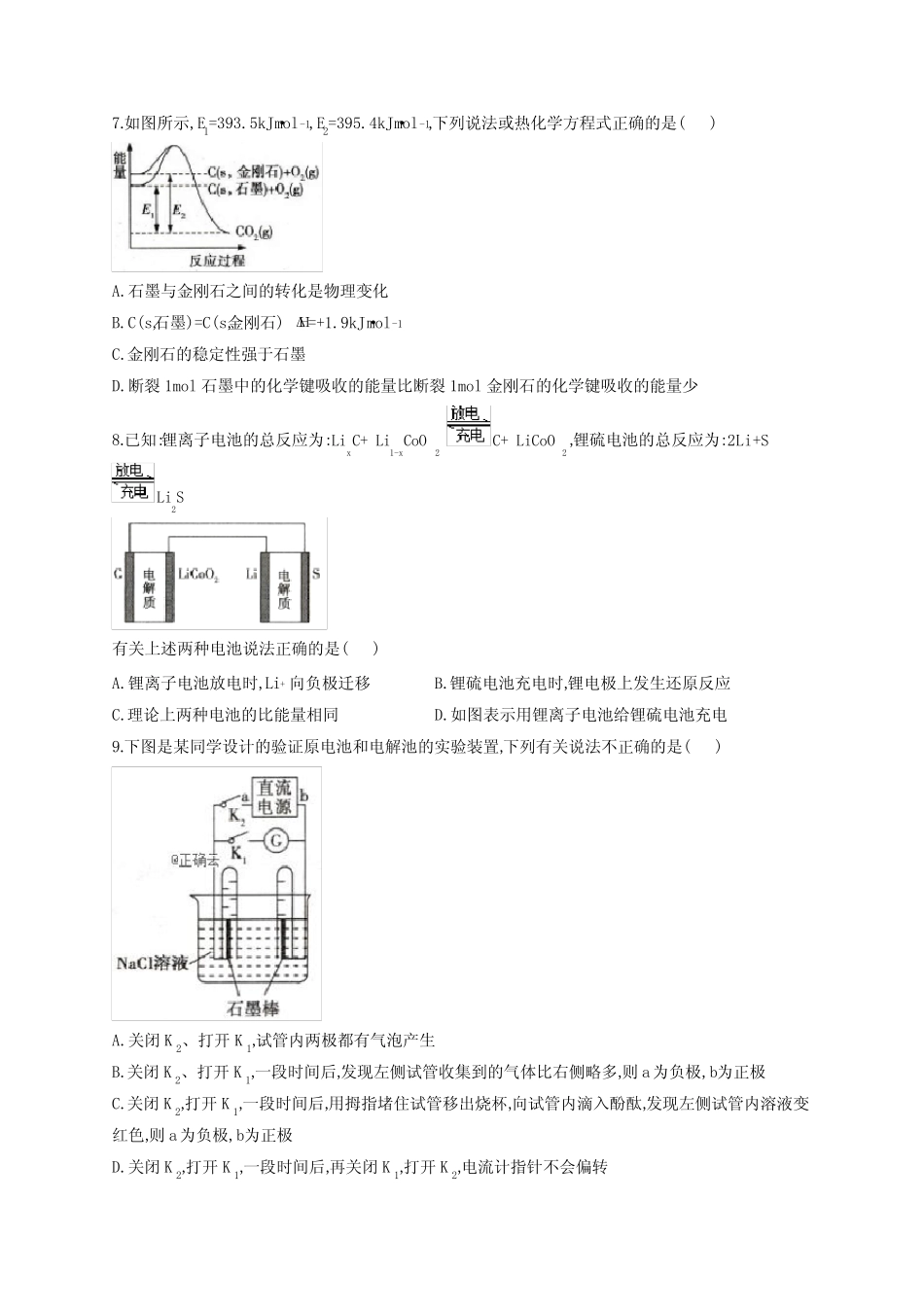
CO和O生成了具有极性共价键的2COD
状态I→状态III表示CO与2O反应的过程2
如图所示,a、b是石墨电极,通电一段时间后,b极附近溶液显红色
下列说法正确的是()A
X极是电源负极,Y极是电源正极B
a极上的电极反应是2Cl--2e-=Cl2↑C
电解过程中CuSO4溶液的pH逐渐增大D
b极上产生2
24L(标准状况下)气体时,Pt极上有6
4gCu析出3
海洋电池以铝合金为电池负极,金属(Pt、Fe)网为正极,科学家把正极制成仿鱼鳃的网状结构
它以海水为电解质溶液,靠海水中的溶解氧与铝反应产生电能
海水中只含有0
5%的溶解氧
不放入海洋时,铝极就不会在空气中被氧化,可以长期储存
用时,把电池放入海水中,便可供电,电池设计使用周期可长达一年以上,避免经常更换电池的麻烦
即使更换,也只是换一块铝合金板,电池总反应式:22436AlOHO34AlOH
下列说法错误的是()A
负极铝被氧化B
海水温度升高,电池反应速率可能加快C
正极制成仿鱼鳃的网状结构的目的是增大正极材料和氧气的接触面积D
正极电极反应式为244OHe22HO4
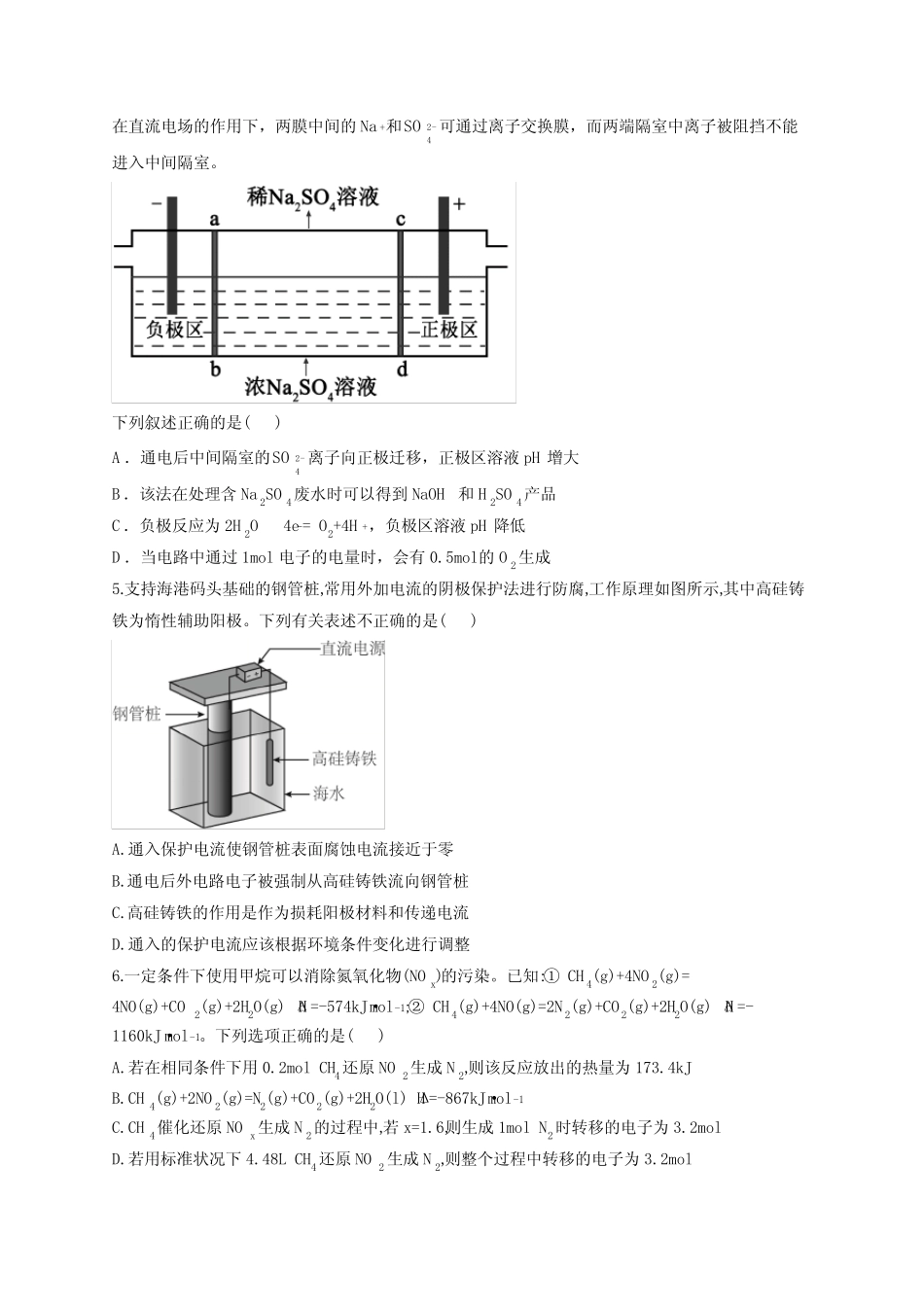
三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和2-4SO可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室
下列叙述正确的是()A.通电后中间隔室的2-4SO离子向正极迁移,正极区溶液pH增大B.该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品C.负极反应为2H2O−4e–=O2+4H+,负极区