专题强化练习(八)化学反应速率和化学平衡1.将BaO2放入密闭的真空容器中,反应2BaO2(s)2BaO(s)+O2(g)达到平衡
保持温度不变,缩小容器容积,体系重新达到平衡,下列说法不正确的是()A.平衡常数不变B.BaO量不变C.氧气压强不变D.BaO2量增加解析:平衡常数只与温度有关,温度不变,平衡常数不变,A正确;保持温度不变,缩小容器容积,也就增大了压强,根据平衡移动原理,化学平衡向气体体积减小的方向移动,即向逆反应方向移动,所以BaO的量减小,B不正确;温度不变,平衡常数不变,其数值等于氧气的浓度,浓度不变,因此压强不变,正确;缩小容器容积,平衡逆向移动,故体系重新达到平衡BaO2量增加,D正确
答案:B2.反应COCl2(g)CO(g)+Cl2(g)ΔH>0,达到平衡时,下列措施:①升温②恒容通入惰性气体③增加CO浓度④减压⑤加催化剂⑥恒压通入惰性气体,能提高COCl2转化率的是()A.①②④B.①④⑥C.②③⑤D.③⑤⑥解析:能提高反应物转化率的方法是在不改变该反应物起始量的条件下使化学平衡向正反应方向移动
①升温向吸热方向即正反应方向移动;②恒容通入惰性气体,各组分浓度不变,平衡不移动;③增加CO浓度使平衡逆向移动;④减压使平衡正向移动;⑤催化剂不影响平衡;⑥恒压通入惰性气体,参与反应的各组分压强减小,平衡正向移动,故①④⑥符合题意
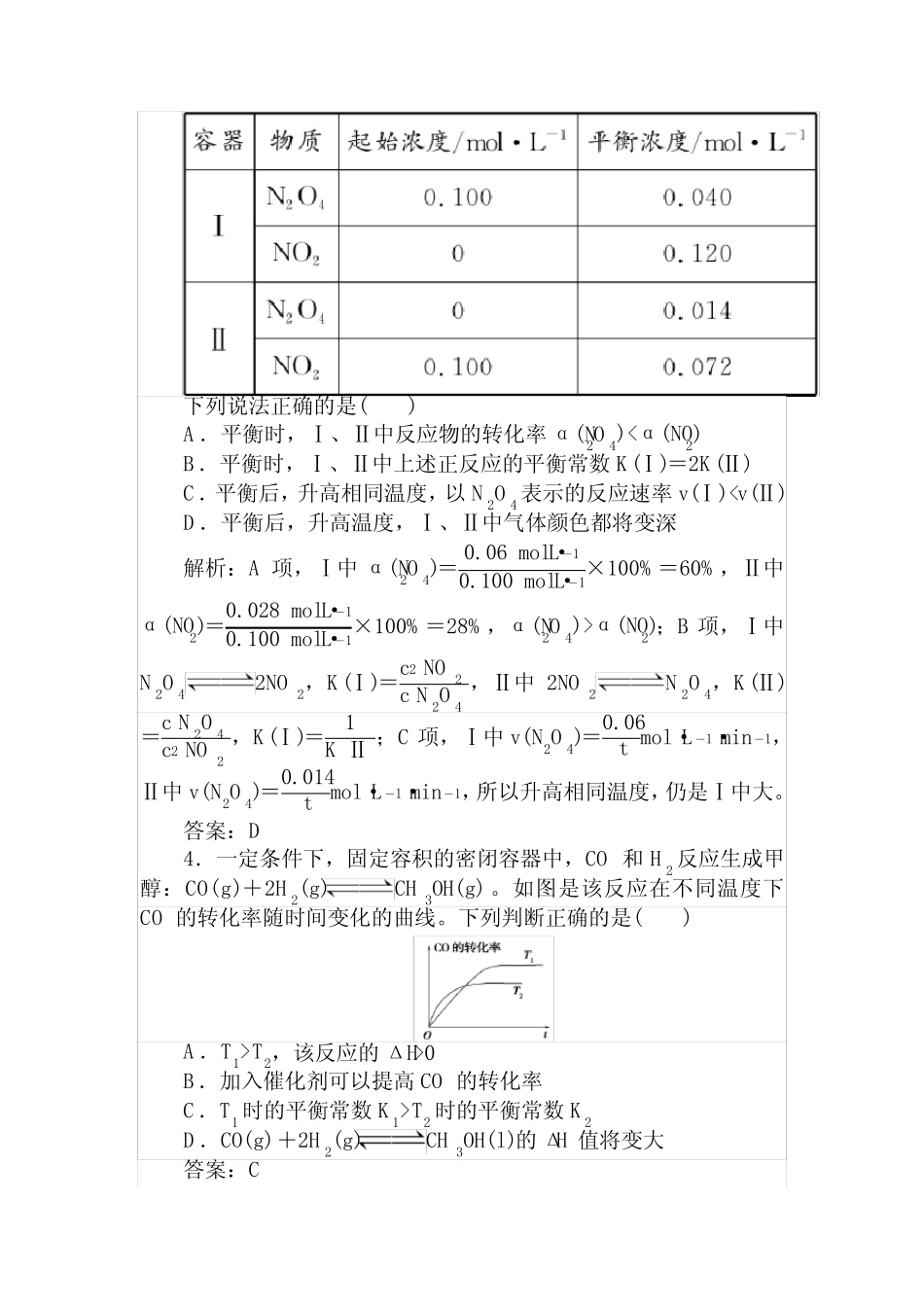
答案:B3.在100℃时,将N2O4、NO2分别充入两个各为1L的密闭容器中,反应过程中浓度变化如下:下列说法正确的是()A.平衡时,Ⅰ、Ⅱ中反应物的转化率α(N2O4)T2,该反应的ΔH>0B.加入催化剂可以提高CO的转化率C.T1时的平衡常数K1>T2时的平衡常数K2D.CO(g)+2H2(g)CH3OH(l)的ΔH值将变大答案:C5.已知反应X(g)+Y(g)nZ(g)ΔH>0,将X和Y以一定比例混合通入密闭容器中进行