一、选择题1.键能是化学键断开需吸收的能量或形成所放出的能量
N4在21世纪才被发现,跟你们的年龄差不多
N4是正四面体结构,有六个N-N单键,N-N键能为193kJ/mol,而N2有一个NN键,键能为946kJ/mol
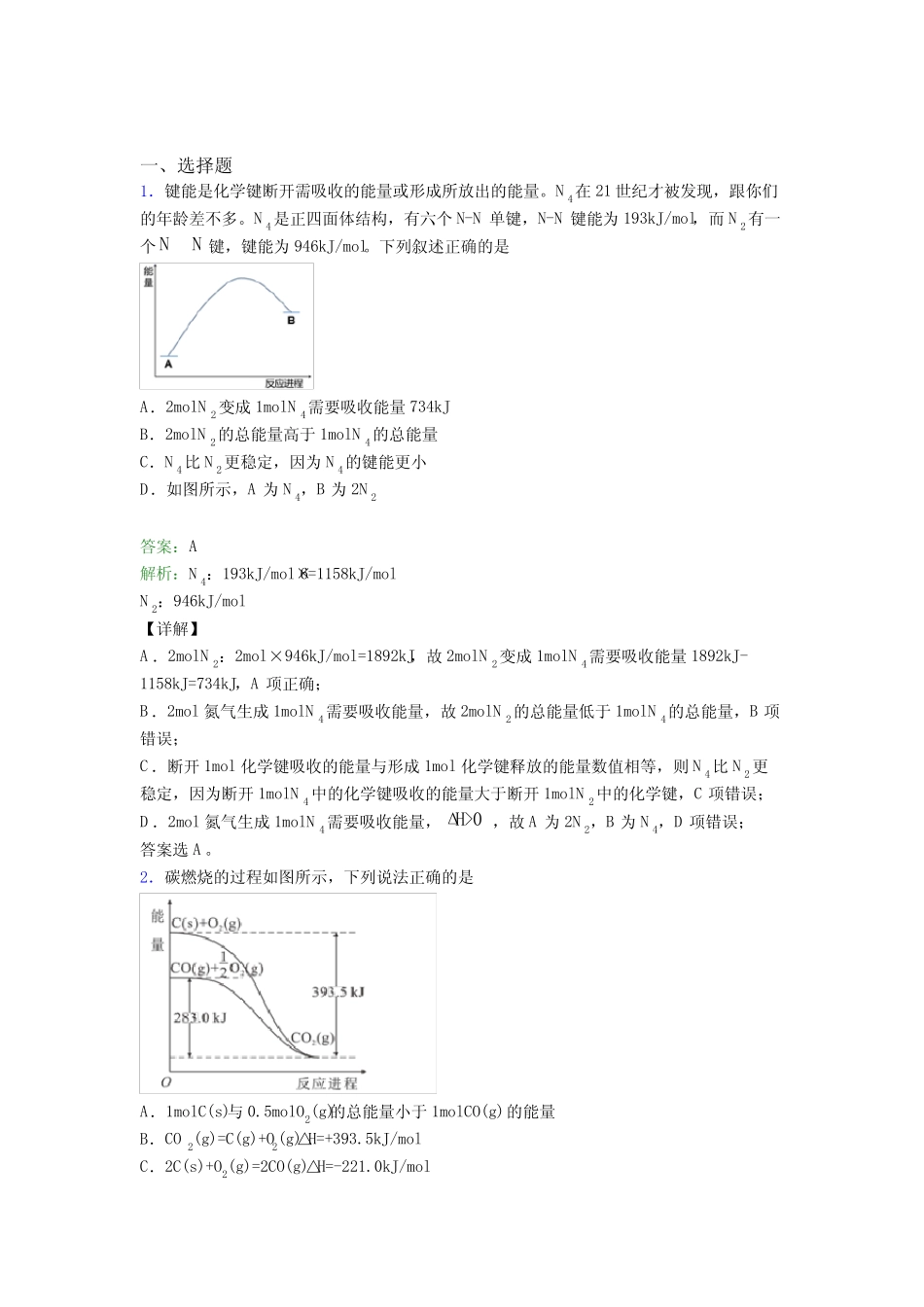
下列叙述正确的是A.2molN2变成1molN4需要吸收能量734kJB.2molN2的总能量高于1molN4的总能量C.N4比N2更稳定,因为N4的键能更小D.如图所示,A为N4,B为2N2答案:A解析:N4:193kJ/mol×6=1158kJ/molN2:946kJ/mol【详解】A.2molN2:2mol×946kJ/mol=1892kJ,故2molN2变成1molN4需要吸收能量1892kJ-1158kJ=734kJ,A项正确;B.2mol氮气生成1molN4需要吸收能量,故2molN2的总能量低于1molN4的总能量,B项错误;C.断开1mol化学键吸收的能量与形成1mol化学键释放的能量数值相等,则N4比N2更稳定,因为断开1molN4中的化学键吸收的能量大于断开1molN2中的化学键,C项错误;D.2mol氮气生成1molN4需要吸收能量,ΔH>0,故A为2N2,B为N4,D项错误;答案选A
2.碳燃烧的过程如图所示,下列说法正确的是A.1molC(s)与0
5molO2(g)的总能量小于1molCO(g)的能量B.CO2(g)=C(g)+O2(g)△H=+393
5kJ/molC.2C(s)+O2(g)=2CO(g)△H=-221
0kJ/molD.等量的碳燃烧C(s)→CO2(g)过程比C(S)→CO(g)→CO2(g)过程释放的能量多答案:C解析:从图中可以看出,C和2O反应属于放热反应,热化学方程式为22C(s)+O(g)=CO(g)=-393
5kJ/molH,同理可得221CO(g)+O(g)=CO(g)=-283