高中化学化学平衡、转化率、平衡移动练习题一、单选题1
一定量的2CO与足量的碳在体积可变的恒压密闭容器中反应:2C(s)+CO(g)2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:已知:气体分压(p分)=气体总压(p总)×体积分数
下列说法正确的是()A
550℃时,若充入惰性气体,v正、v逆均减小,平衡不移动B
650℃时,反应达平衡后2CO的转化率为25
T℃时,若充入等体积的2CO和CO,平衡向逆反应方向移动D
925℃时,用平衡分压代替平衡浓度表示的化学平衡常数p24
0Kp总2
可逆反应①X(g)+2Y(g)2Z(g)、②2M(g)N(g)+P(g),分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板
反应开始和达到平衡状态时有关物理量的变化如图所示:下列判断正确的是()A
反应①的正反应是吸热反应B
达平衡(Ⅰ)时体系的压强和反应开始时体系的压强之比为14:15C
达平衡(Ⅰ)时,X的转化率为511D
在平衡(Ⅰ)和平衡(Ⅱ)中,M的体积分数相等3
将物质的量均为3
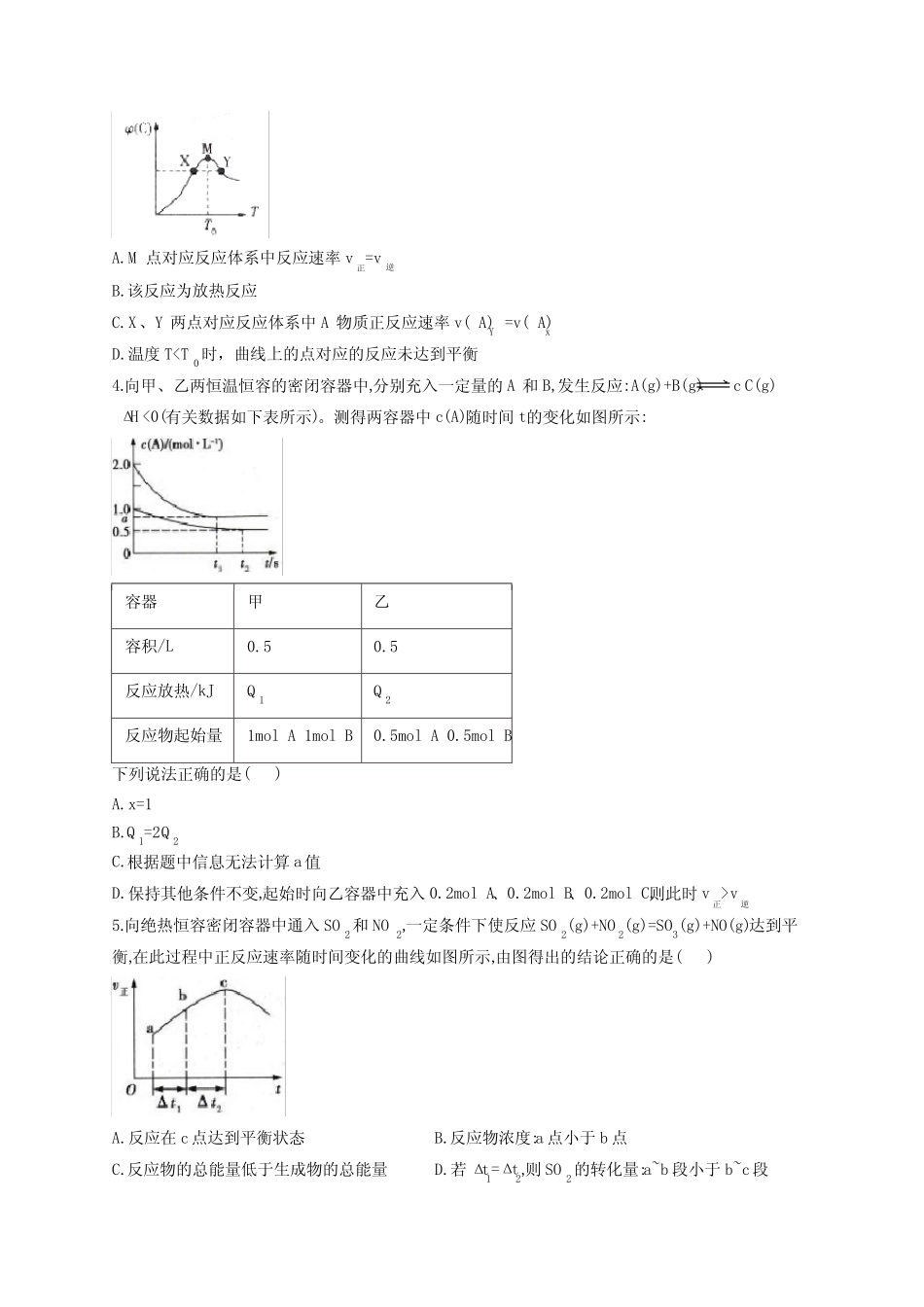
00mol的气体A、B充入5L恒容密闭容器中,发生如下反应3A(g)+B(g)==C(g)他条件一定时,反应过程中C的物质的量分数(C)随温度T的变化曲线如图所示,下列有关说()A
M点对应反应体系中反应速率v正=v逆B
该反应为放热反应C
X、Y两点对应反应体系中A物质正反应速率v(A)Y=v(A)xD