专题十一化学反应速率和化学平衡综合篇综合分压平衡常数(Kp)的计算1
(2019课标Ⅱ,27节选)环戊二烯()是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产
回答下列问题:(1)已知:(g)(g)+H2(g)ΔH1=100
3kJ·mol-1①H2(g)+I2(g)2HI(g)ΔH2=-11
0kJ·mol-1②对于反应:(g)+I2(g)(g)+2HI(g)③ΔH3=kJ·mol-1
(2)某温度下,等物质的量的碘和环戊烯()在刚性容器内发生反应③,起始总压为105Pa,平衡时总压增加了20%,环戊烯的转化率为,该反应的平衡常数Kp=Pa
达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有(填标号)
通入惰性气体B
增加环戊烯浓度D
增加碘浓度(3)环戊二烯容易发生聚合生成二聚体,该反应为可逆反应
不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是(填标号)
T1>T2B
a点的反应速率小于c点的反应速率C
a点的正反应速率大于b点的逆反应速率D
b点时二聚体的浓度为0
45mol·L-1答案(1)+89
3(2)40%3
56×104BD(3)CD2
(2020课标Ⅲ,28,14分)二氧化碳催化加氢合成乙烯是综合利用CO2的热点研究领域
回答下列问题:(1)CO2催化加氢生成乙烯和水的反应中,产物的物质的量之比n(C2H4)∶n(H2O)=
当反应达到平衡时,若增大压强,则n(C2H4)(填“变大”“变小”或“不变”)
(2)理论计算表明,原料初始组成n(CO2)∶n(H2)=1∶3,在体系压强为0
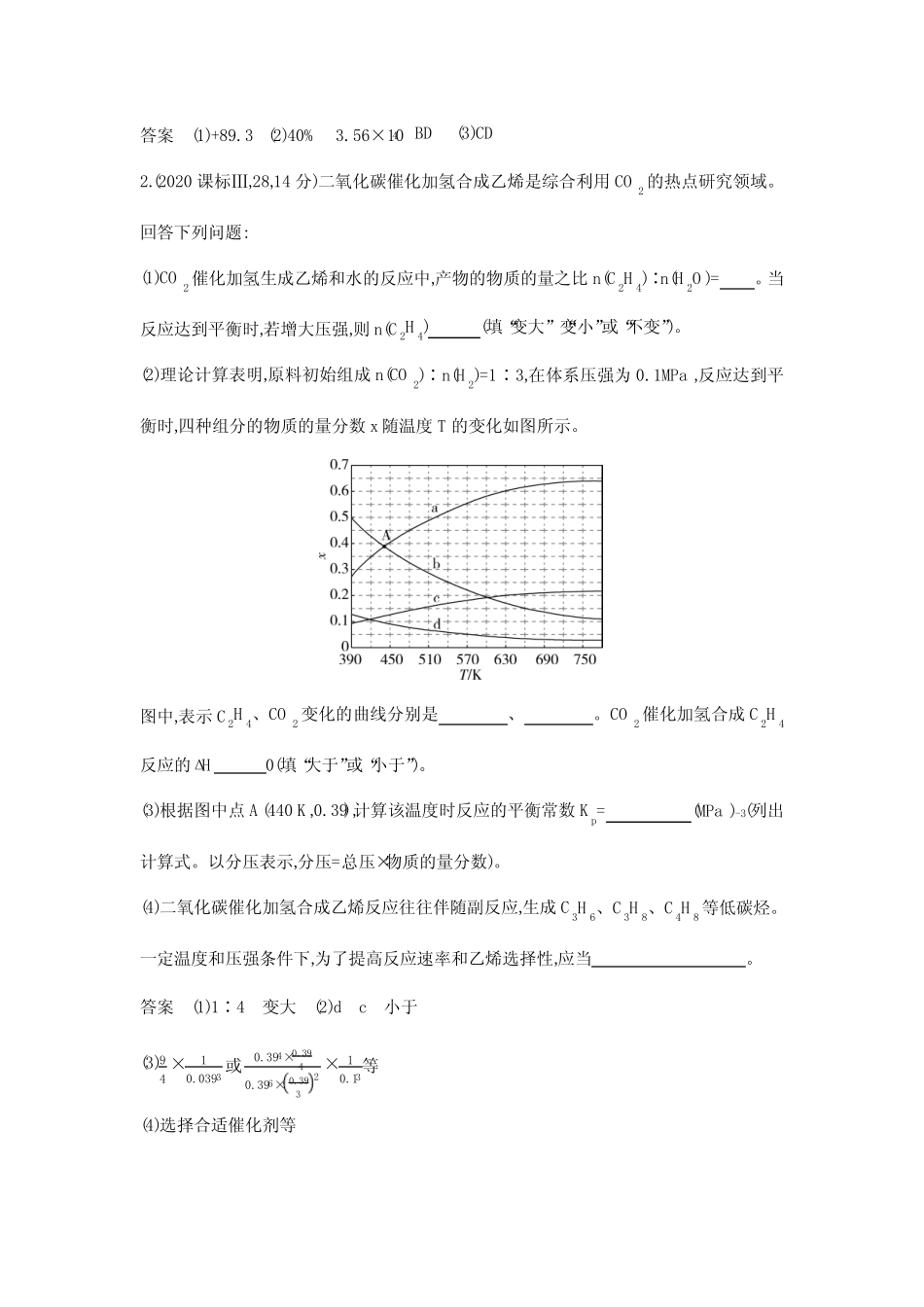
1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示
图中,表示C2H4、CO2变化的曲线分别是、
CO2催化加氢合成C2H4反应的ΔH0(填“大于”或“小于”)
(3)根据图中点A(440K,0