1课时35晶体结构与性质(本课时对应学生用书第158~161页)【课时导航】复习目标1
了解NaCl型和CsCl型离子晶体的结构特征,能用晶格能解释典型离子化合物的某些物理性质
了解原子晶体的特征,能描述金刚石、二氧化硅等原子晶体的结构与性质的关系
能用金属键的自由电子理论解释金属的某些物理性质
知道金属晶体的基本堆积方式,了解常见金属晶体的晶胞结构特征
知道分子晶体的含义,了解分子间作用力的大小对物质某些物理性质的影响
了解分子晶体与原子晶体、离子晶体、金属晶体的结构微粒、微粒间作用力的区别
知识网络问题思考问题1准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,通过什么方法可以区别晶体、准晶体和非晶体
问题2NaCl、CsCl、金属晶体、金刚石、干冰晶体的配位数是多少
【自主学习】考点1常见晶体与晶体类型的判断【基础梳理】1
晶胞:是描述晶体结构的基本单元,晶胞是从晶体中“截取”出来具有代表性的重复单位
晶胞在晶体中的排列呈“无隙并置”
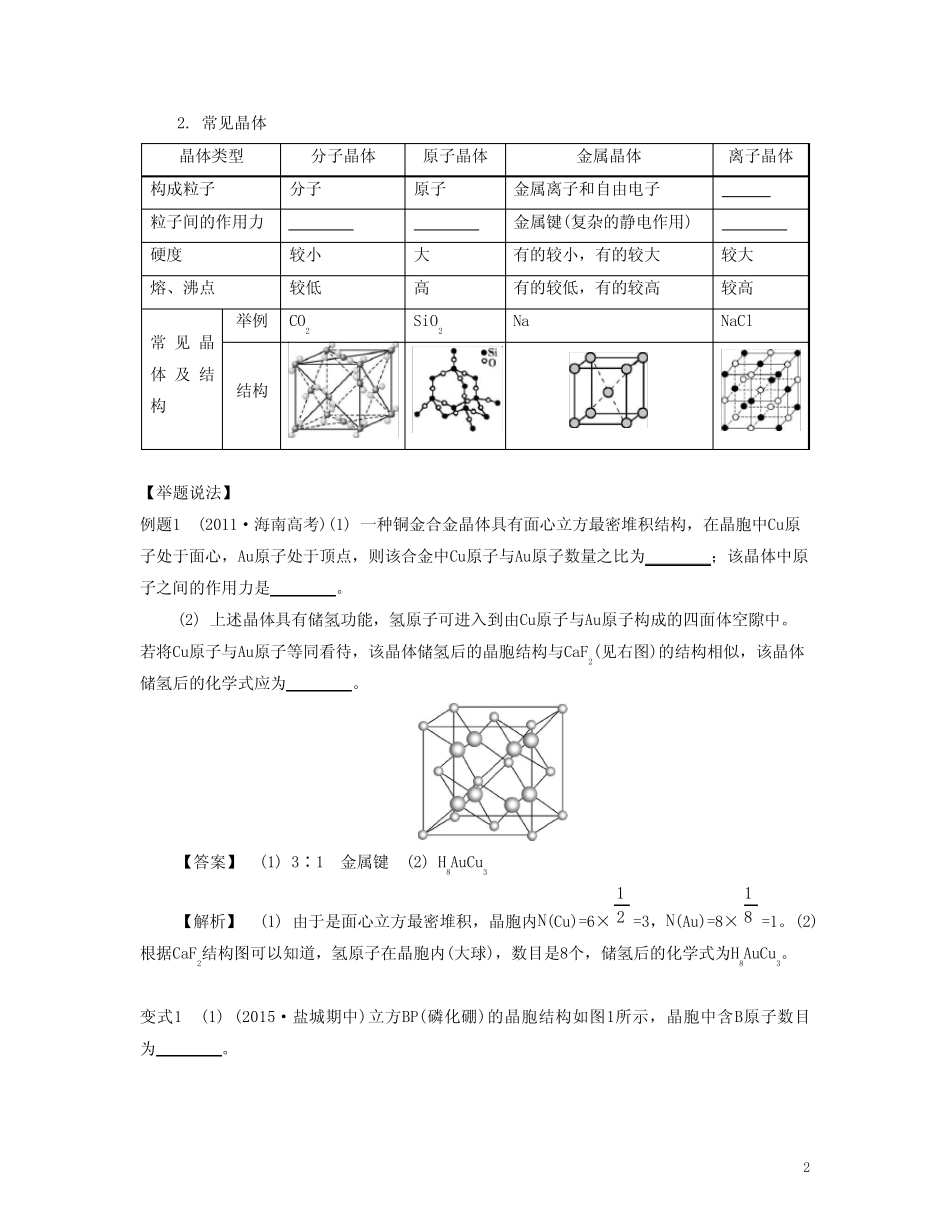
常见晶体晶体类型分子晶体原子晶体金属晶体离子晶体构成粒子分子原子金属离子和自由电子粒子间的作用力金属键(复杂的静电作用)硬度较小大有的较小,有的较大较大熔、沸点较低高有的较低,有的较高较高常见晶体及结构举例CO2SiO2NaNaCl结构【举题说法】例题1(2011·海南高考)(1)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中Cu原子处于面心,Au原子处于顶点,则该合金中Cu原子与Au原子数量之比为;该晶体中原子之间的作用力是
(2)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中
若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2(见右图)的结构相似,该晶体储氢后的化学式应为
【答案】(1)3∶1金属键(2)H8AuCu3【解析】(1)由于是面心立方最密堆积