从铝土矿到铝合金镁[江苏考纲要求]—————————————————————————————————————1.理解并能应用常见金属的活动顺序
2.了解常见金属铝及其重要化合物的主要性质和重要应用
3.认识化学在金属矿物等自然资源综合利用和实现物质间转化等方面的实际应用
4.了解金属材料在生产和生活中的重要应用
认识常见无机物在生产中的应用和对生态环境的影响
[教材基础—自热身]1.铝的物理性质(1)位置与地位铝元素处在周期表中第三周期第ⅢA族,在地壳中含量仅次于硅,是地壳中含量最多的金属元素,在自然界中以化合态存在
(2)物理性质色态密度质地银白色,有金属光泽固体较小较软2
掌握铝的化学性质与用途(1)铝的化学性质铝的原子结构示意图为,其最外层有3个电子,决定了其金属性相对活泼,能与非金属、酸等发生反应
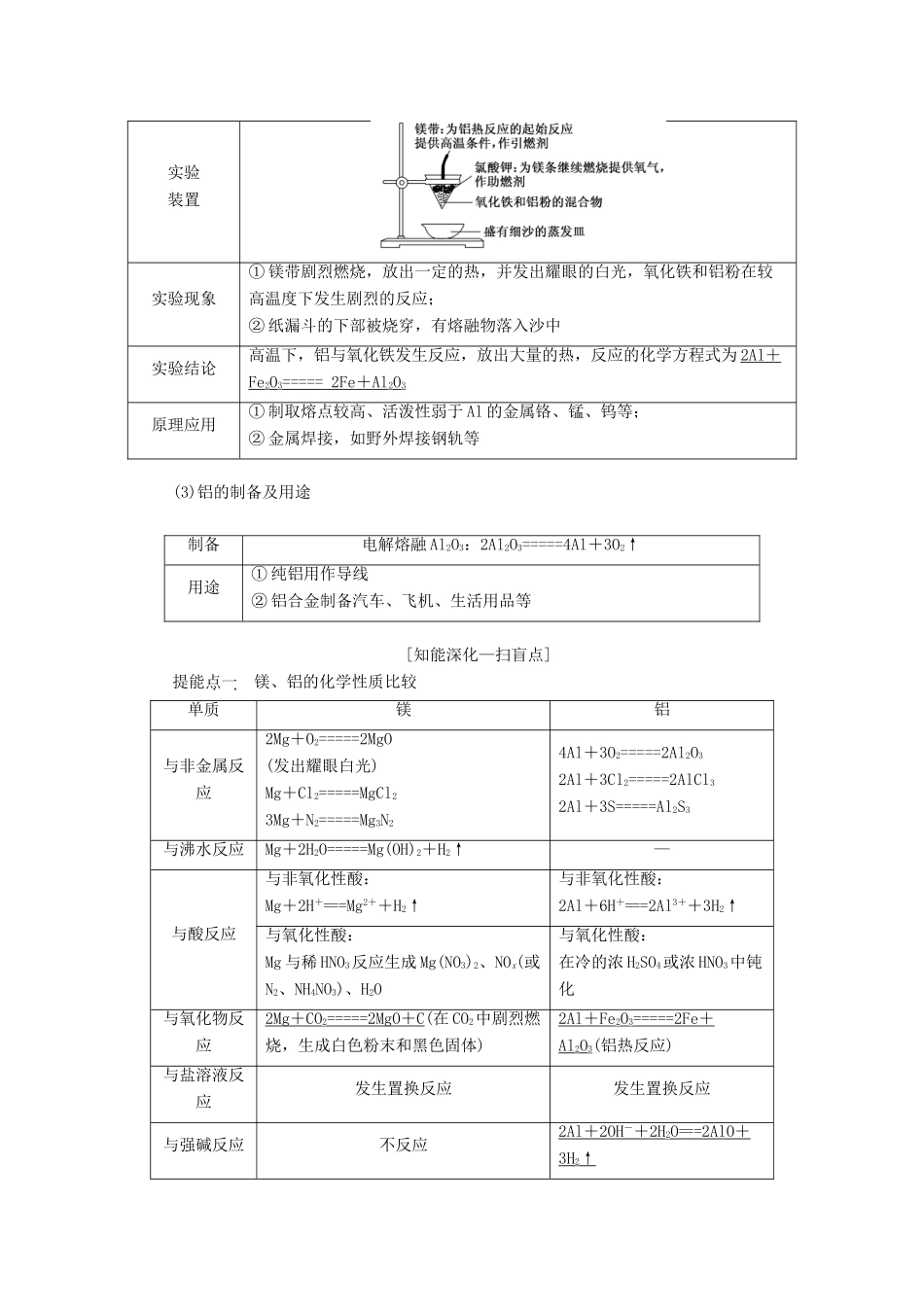
与非金属反应(O2、Cl2)与O2反应与Cl2反应:2Al+3Cl2=====2AlCl3与酸反应常温下,Al与浓硫酸、浓硝酸发生钝化,而遇稀的强氧化性稀HNO3:Al+NO+4H+===Al3++NO↑+2H2O非氧化性酸(盐酸或稀H2SO4):2Al+6H+===2Al3++3H2↑与强碱反应(NaOH)2Al+2OH-+2H2O===2AlO+3H2↑与氧化物反应(Fe2O3)2Al+Fe2O3=====2Fe+Al2O3(铝热反应)(2)铝热反应镁、铝的性质及应用实验装置实验现象①镁带剧烈燃烧,放出一定的热,并发出耀眼的白光,氧化铁和铝粉在较高温度下发生剧烈的反应;②纸漏斗的下部被烧穿,有熔融物落入沙中实验结论高温下,铝与氧化铁发生反应,放出大量的热,反应的化学方程式为2Al+Fe2O3=====2Fe+Al2O3原理应用①制取熔点较高、活泼性弱于Al的金属铬、锰、钨等;②金属焊接,如野外焊接钢轨等(3)铝的制备及用途制备电解熔融Al2O3:2Al2O3=====