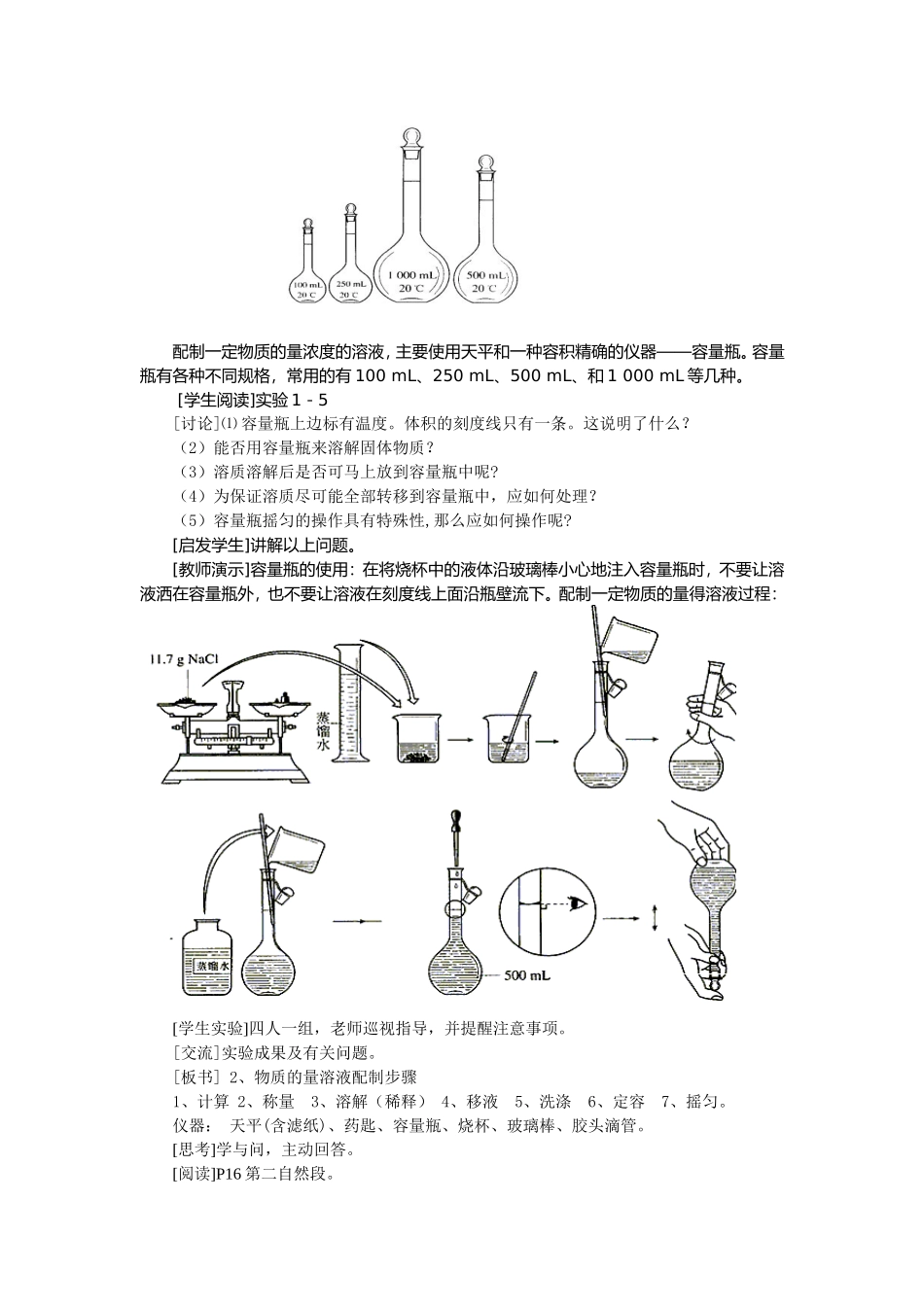
第二节化学计量在实验中的应用(第二课时)教学目标:1、使学生理解物质的量浓度的概念;会运用物质的量浓度的概念进行简单的计算;学会配制物质的量浓度溶液的方法和技能
2、从概念的应用中,培养学生实验能力和思维能力
培养学生发现问题和解决问题的能力
情感目标:1、通过概念的学习和溶液的配制,培养学生理论联系实际的学习自然科学的思想
2、培养学生学习自然科学的学习兴趣以及严谨求实的学习态度
教学重点:一定物质的量浓度的溶液的配制方法
实验准备:天平(含滤纸)、药匙、容量瓶、烧杯、玻璃棒、胶头滴管各15套
教学过程:[复习]物质的质量、物质的量、摩尔质量之间的相互转化关系N/NA=n=m/M[导入新课]我们在初中学习过溶液中溶质的质量分数,应用这种表示溶液浓度的方法,可以计算一定质量的溶液中所含溶质的质量
但是,很多化学反应都在溶液中进行,对于溶液我们通常不称其质量,而是量它的体积
同时,在化学反应中,反应物与生成物物质的量相互间有一定的关系
[板书]二、物质的量在化学实验中的作用[自主探究]如何设置一个物理量,使物质的量和体积联系起来
注意以下几点:1、可以表示体积,我们最取一定体积时通过这个物理量就可以知道很快地知道它的物质的量
2、我们要取若干物质的量的溶质时,通过这个物理量就可以知道要量取多少体积的溶液
[总结]通常我们把这个物理量称为物质的量浓度
即[阅读]P14相关内容[板书]]1、物质的量浓度:单位体积溶液中所含溶质B的物质的量,又叫B的物质的量浓度,符号CB,公式:CB=nB/V,单位通常是用mol/L表示
[讲述]1、溶液体积为1升,而不是溶剂体积是1升;2、溶质是用物质的量表示,而不是用摩尔质量表示
[讲解]例题:1、用5molNaOH配成500mL溶液,其浓度为___mol/L,取5mL该溶液,其浓度为___mol/L
2、从1L1mol/LNaCl溶液中,分别