第三课时[问题情境]C、Si同属ⅣA元素,且上下相邻,应具相似的性质
今已知CO2的晶体为分子晶体,熔、沸点很低
那么SiO2晶体是否具有与其相似的结构和性质呢
[投影]CO2和SiO2一些性质的比较[分析]两者相比,性质差异很大
由SiO2很高的熔、沸点,可推知它不属于分子晶体
其质点粒子不是分子
它是离子晶体吗
从其元素组成和化合物类别看,SiO2不是离子化合物
它属于我们本节要学习的一类晶体
[板书]三、原子晶体[引述]SiO2和CO2性质的差别缘于两者结构的不同
[展示]SiO2的晶体结构模型
[观察并思考]1
构成SiO2晶体的粒子是什么
粒子通过何种方式结合
怎样构成晶体
[讲述]构成SiO2晶体的粒子是中性原子,原子与原子间以共价键相结合
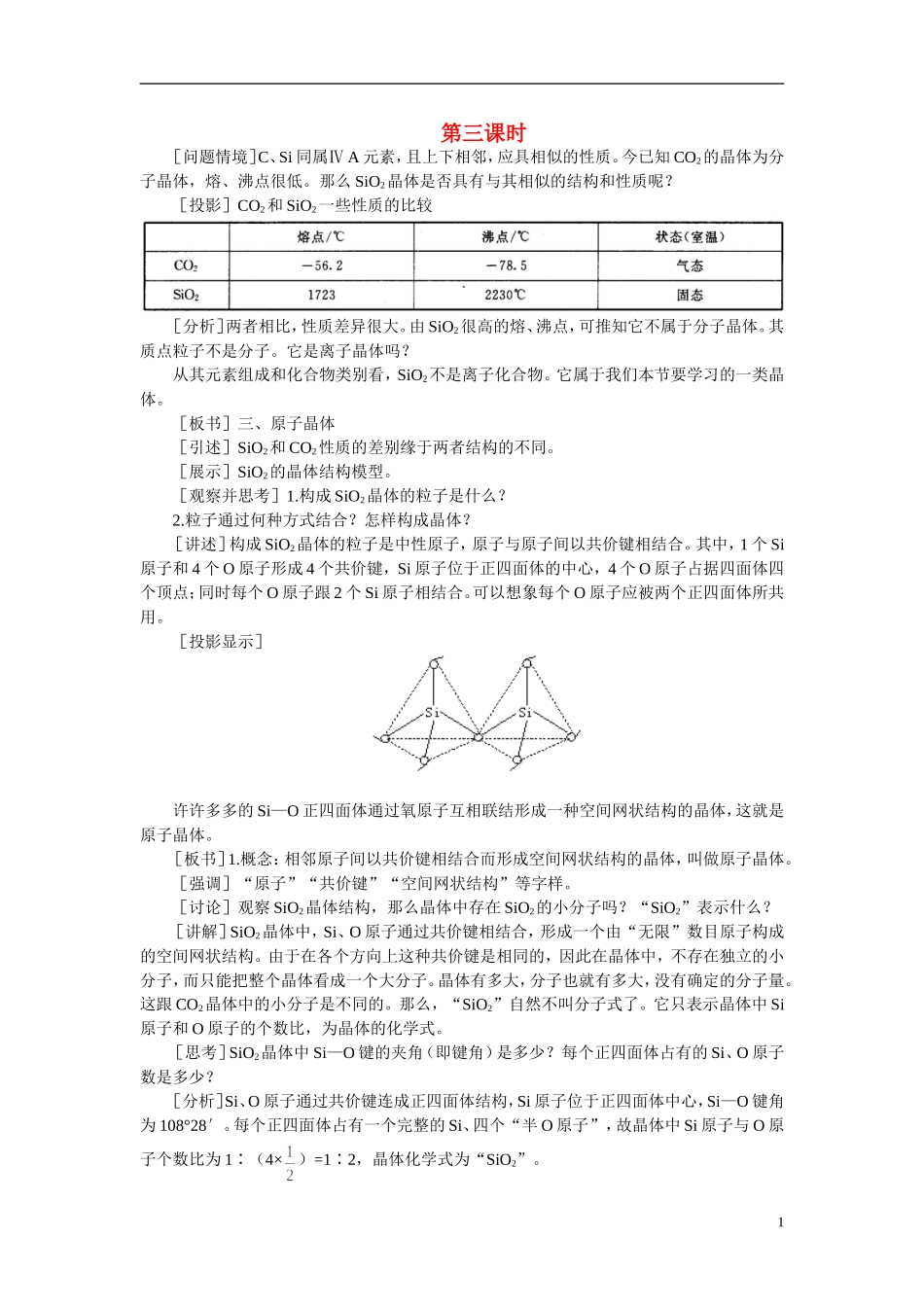
其中,1个Si原子和4个O原子形成4个共价键,Si原子位于正四面体的中心,4个O原子占据四面体四个顶点;同时每个O原子跟2个Si原子相结合
可以想象每个O原子应被两个正四面体所共用
[投影显示]许许多多的Si—O正四面体通过氧原子互相联结形成一种空间网状结构的晶体,这就是原子晶体
概念:相邻原子间以共价键相结合而形成空间网状结构的晶体,叫做原子晶体
[强调]“原子”“共价键”“空间网状结构”等字样
[讨论]观察SiO2晶体结构,那么晶体中存在SiO2的小分子吗
“SiO2”表示什么
[讲解]SiO2晶体中,Si、O原子通过共价键相结合,形成一个由“无限”数目原子构成的空间网状结构
由于在各个方向上这种共价键是相同的,因此在晶体中,不存在独立的小分子,而只能把整个晶体看成一个大分子
晶体有多大,分子也就有多大,没有确定的分子量
这跟CO2晶体中的小分子是不同的
那么,“SiO2”自然不叫分子式了
它只表示晶体中Si原子和O原子的个数比,为晶体的化学式
[思考]SiO2晶体中Si—O键的夹角(即键角)是多少