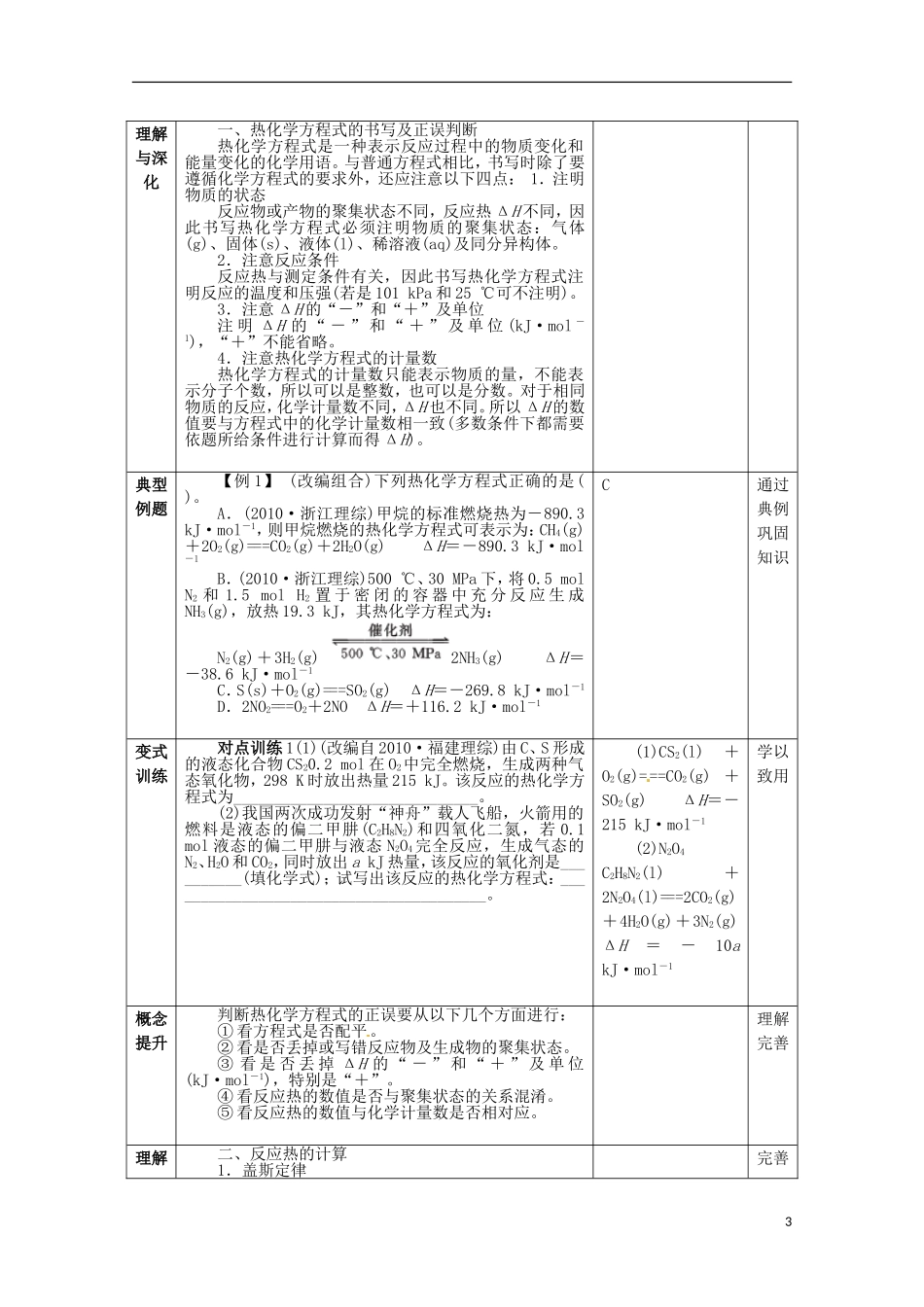
山东省枣庄八中高二化学《化学反应的热效应课型:复习教学模式:问题探究式教学教学目标:1
了解化学反应中能量转化的原因,能说出常见的能量转化形式
2.了解化学能与热能的相互转化
了解吸热反应、放热反应、反应热等概念
3.了解热化学方程式的含义,能用盖斯定律进行有关反应热的简单计算
4.了解能源是人类生存和社会发展的重要基础
了解化学在解决能源危机中的重要作用
内容分析:这部分内容中有许多考点是每年高考的必考内容
主要有以下几点:1.书写热化学方程式或判断热化学方程式的正误;2.有关反应热的计算;放热反应、吸热反应的判断
3.比较反应热的大小,结合反应热分析化学反应速率、化学平衡基本规律
4.反应热跟化学键的综合联系
最近又出现反应热与能源结合起来进行考查
由于能源问题已成为社会热点,有关能源的试题也将成为今后命题的重点:预计考查反应热的内容将不断拓宽,难度有所提高,题型也会有新的变化
教学过程:环节教师活动学生活动设计意图情景引入导学诱思下列反应属于吸热反应的是____
①反应物的总能量大于生成物的总能量;②ΔH>0;③发生反应时,断开反应物的化学键吸收的总能量大于生成生成物时形成新化学键放出的总能量;④所有的燃烧反应
阅读教材思考、讨论确定正确的结论
②③通过回答问题,了解掌握情况交流研讨教材回归1.定义:________________
2.符号:________
3.单位:______________
4.产生原因吸收能量E1↓反应物――→生成物↓放出能量E25.表示(1)吸热反应:ΔH为“____”或ΔH____0
(2)放热反应:ΔH为“____”或ΔH____0
6.常见的放热反应和吸热反应放热反应吸热反应学生思考回答1.化学反应放出或吸收的能量2.ΔH3.kJ·mol-14.吸热放热5.+>-