CuC氯化铁溶液化学能转化为电能——电池(第一课时)教材分析:了解反应中的能量变化,体验化学能与电能转化过程,了解氧化还原反应的实质,了解电解池的工作原理,能写出常见原电池的电极反应和电池的化学反应方程式,了解常见化学电源的种类及工作原理
本节在高考中占有重要地位
本节重点原电池的工作原理和组成条件,难点原电池的工作原理
【学习目标】1、掌握原电池的工作原理,熟练书写电极反应式和电池反应方程式
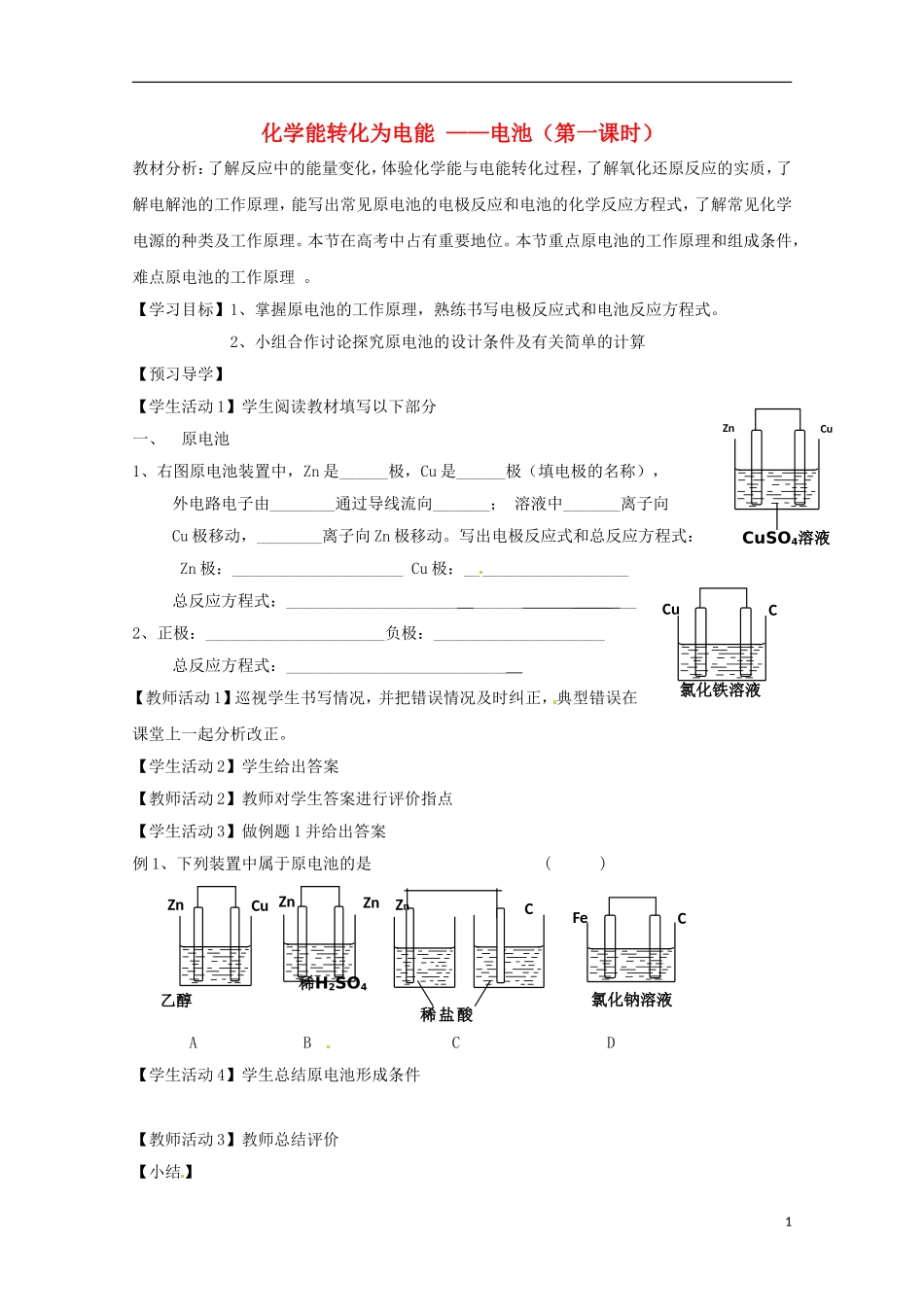
2、小组合作讨论探究原电池的设计条件及有关简单的计算【预习导学】【学生活动1】学生阅读教材填写以下部分一、原电池1、右图原电池装置中,Zn是______极,Cu是______极(填电极的名称),外电路电子由________通过导线流向_______;溶液中_______离子向Cu极移动,________离子向Zn极移动
写出电极反应式和总反应方程式:Zn极:_____________________Cu极:____________________总反应方程式:__________________________________2、正极:______________________负极:_____________________总反应方程式:___________________________【教师活动1】巡视学生书写情况,并把错误情况及时纠正,典型错误在课堂上一起分析改正
【学生活动2】学生给出答案【教师活动2】教师对学生答案进行评价指点【学生活动3】做例题1并给出答案例1、下列装置中属于原电池的是()ABCD【学生活动4】学生总结原电池形成条件【教师活动3】教师总结评价【小结】1ZnCuCuSO4溶液ZnCu乙醇ZnZn稀H2SO4ZnC稀盐酸FeC氯化钠溶液盐桥XYA氯化钠溶液电流计Ag(1)原电池的构成条件:①_________________②_______________