电解原理极其应用(一)网上课堂:[本讲主要内容]一、电解:1.定义:使电流通过电解质而在阴阳两极引起氧化还原反应的过程
2.电解池构成条件:①两个电极②直流电源③电解质溶液或熔融的电解质④构成回路3.电解原理:阳极:失电子,发生氧化反应阴极:得电子,发生还原反应4.离子放电顺序:①阳离子在阴极上放电顺序:Au3+>Ag+>Hg2+>Fe3+>Cu2+>H+>Pb2+>Sn2+>Fe2+>Zn2+>Al3+>Mg2+>Na+>Ca+>K+Fe3+>Cu2+控制一定条件也可在水中放电熔融时放电②阴离子在阳极上放电顺序:A隋性电极(Pt,石墨):S2->I->Br->Cl->OH->,,,F-B非隋性电极(除Pt,Au外的金属):阳极金属本身失去电子形成阳离子进入溶液
二、电解原理的应用:1.电解精炼:粗金属作阳极;纯金属作阴极;含有该离子的水溶液作电解液;通以直流电
2.电流:所镀金属作阳极;镀件作阴极;含镀层离子的水溶液作电解液;通以直流电
电镀只是金属搬家,溶液的浓度和pH均不变
3.氯碱工业:电解饱和食盐水→NaOH,Cl2,H2→化工产品①电极反应:两极:Cl-—2e-=Cl2↑(氧化反应)阴极:2H++2e-=H2↑(还原反应)总:2NaCl+2H2O2NaOH+Cl2↑+H2↑②现象:电极上均有气体放出,阴极产生Cl2有刺激性气味,使润湿的KI-淀粉试纸变蓝;阴极放出H2,向电解后的溶液中滴入酚酞试液,阴极附近溶液颜色变红
③问题:产品为NaOH和Cl2,它们可反应生成NaClO,而H2和Cl2混合遇火爆炸,故应避免产1物混合,需在特殊的电解槽(即离子交换膜电解槽)内进行
[学习指导]1
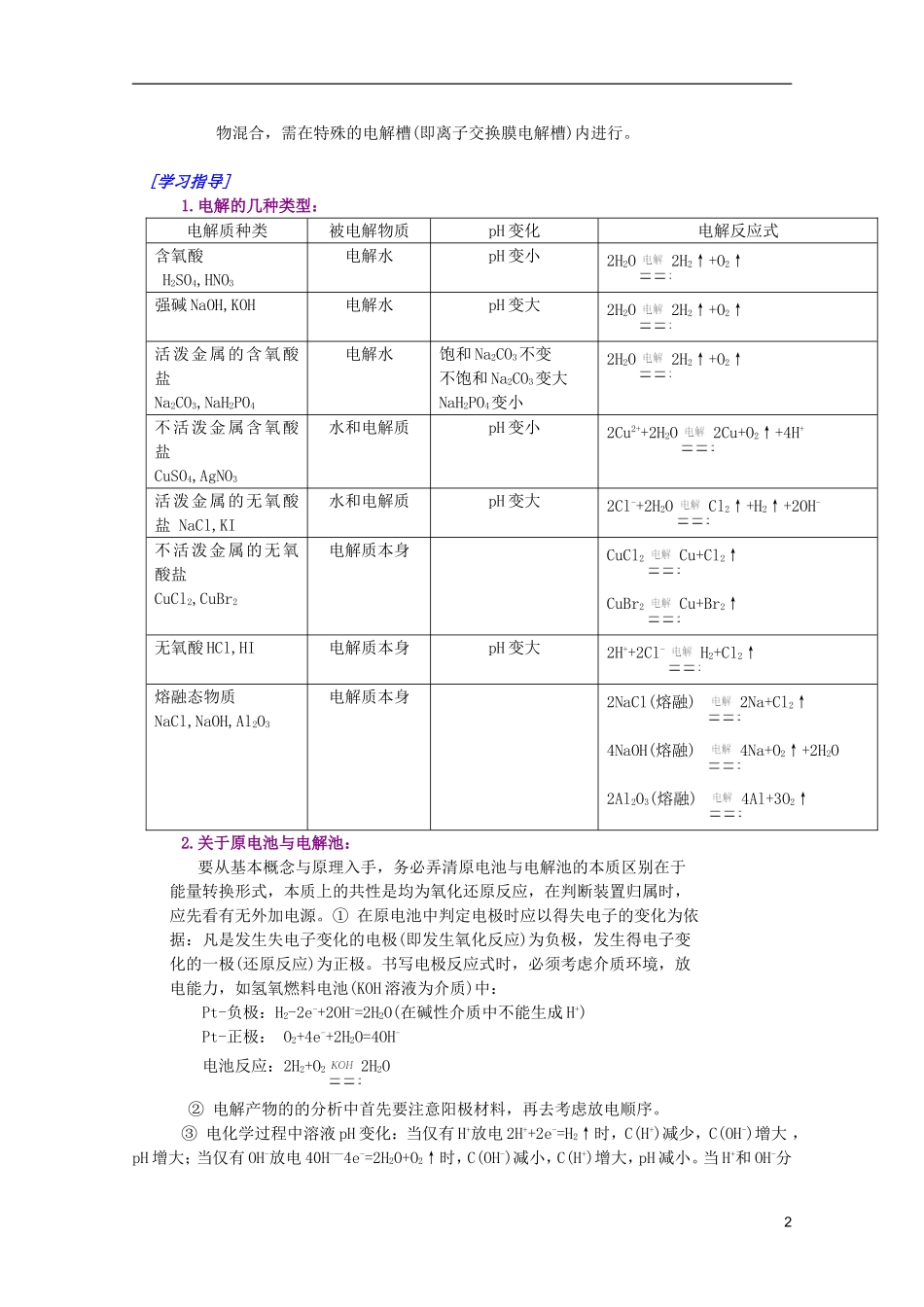
电解的几种类型:电解质种类被电解物质pH变化电解反应式含氧酸H2SO4,HNO3电解水pH变小2H2O2H2↑+O2↑强碱NaOH,KOH电解水pH变大2H2O2H2↑+O2↑活泼