山东省单县职高2013-2014年高中化学2
2分子的立体结构(第1课时)教案新人教版选修3教学目标1、认识共价分子的多样性和复杂性;2、初步认识价层电子对互斥模型;3、能用VSEPR模型预测简单分子或离子的立体结构;4、培养学生严谨认真的科学态度和空间想象能力
重点难点分子的立体结构;利用价层电子对互斥模型预测分子的立体结构教学过程创设问题情境:1、阅读课本P37-40内容;2、展示CO2、H2O、NH3、CH2O、CH4分子的球辊模型(或比例模型);3、提出问题:⑴什么是分子的空间结构
⑵同样三原子分子CO2和H2O,四原子分子NH3和CH2O,为什么它们的空间结构不同
[讨论交流]1、写出CO2、H2O、NH3、CH2O、CH4的电子式和结构式;2、讨论H、C、N、O原子分别可以形成几个共价键;3、根据电子式、结构式描述CO2、H2O、NH3、CH2O、CH4的分子结构
[模型探究]由CO2、H2O、NH3、CH2O、CH4的球辊模型,对照其电子式云哟内分类对比的方法,分析结构不同的原因
[引导交流]引导学生得出由于中心原子的孤对电子占有一定的空间,对其他成键电子对存在排斥力,影响其分子的空间结构
——引出价层电子对互斥模型(VSEPRmodels)[讲解分析]价层电子对互斥模型把分子分成两大类:一类是中心原子上的价电子都用于形成共价键
如CO2、CH2O、CH4等分子中的C原子
它们的立体结构可用中心原子周围的原子数来预测,概括如下:ABn立体结构范例n=2直线型CO21n=3平面三角形CH2On=4正四面体型CH4另一类是中心原子上有孤对电子(未用于形成共价键的电子对)的分子
如H2O和NH3中心原子上的孤对电子也要占据中心原子周围的空间,并参与互相排斥
因而H2O分子呈V型,NH3分子呈三角锥型
(如图)课本P40
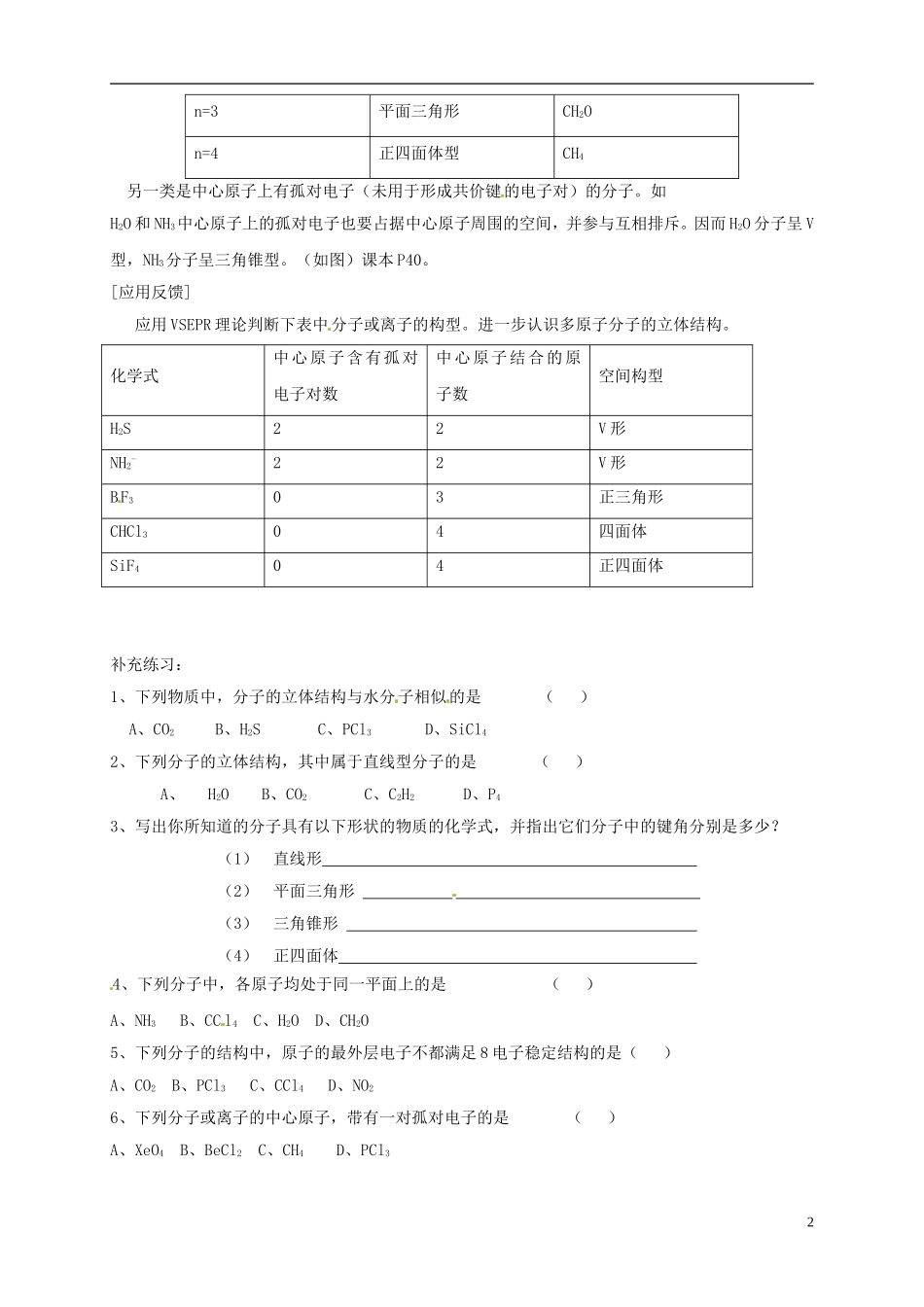
[应用反馈]应用VSEPR理论判断下表中分子或