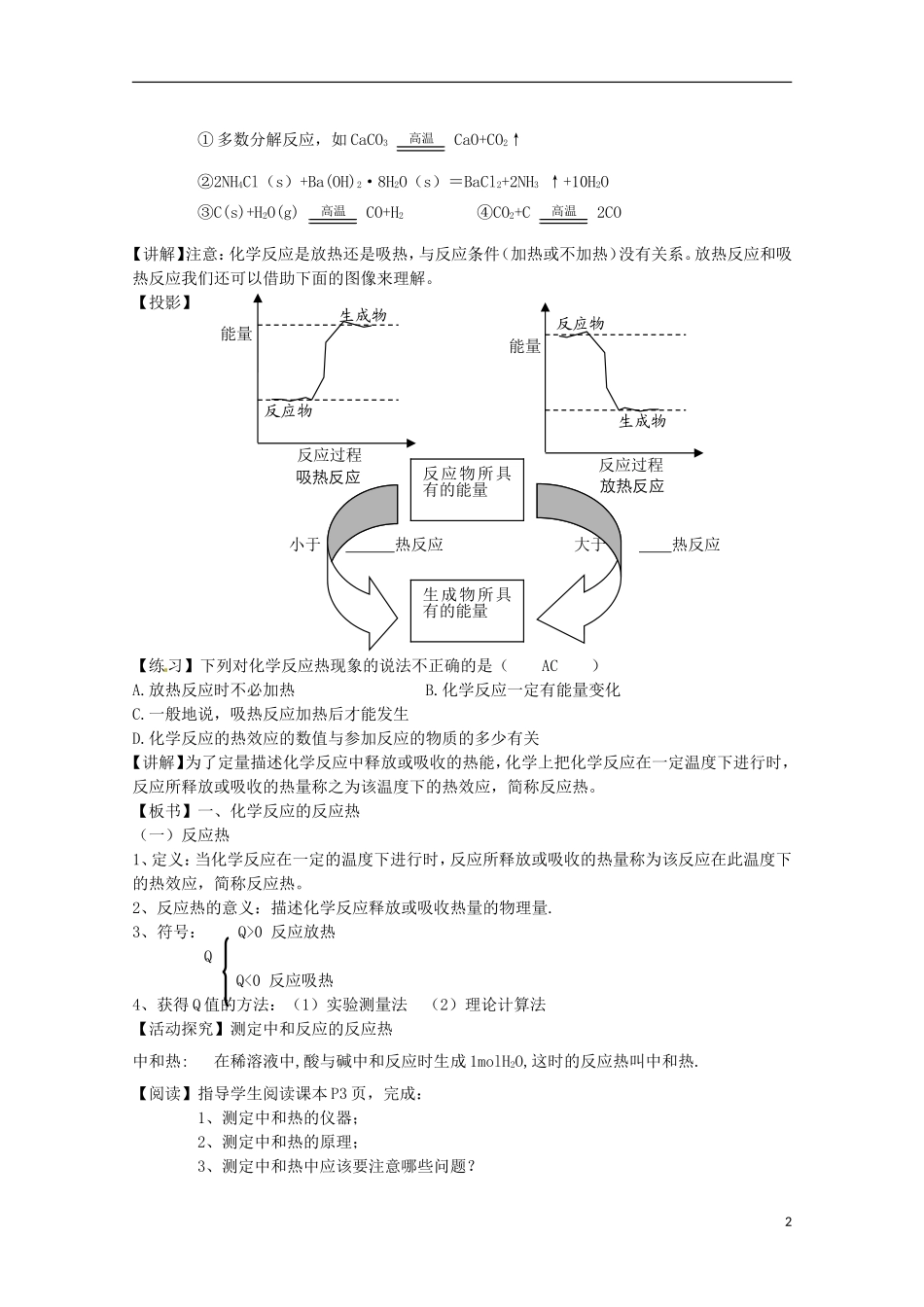
第1节化学反应的热效应【教材分析】本节教材在学习了化学反应中的能量变化的知识基础上,对反应热进一步深化认识,引入含的定义,再进一步分析化学反应中的物质的焓变,最后用热化学方程式表示出反应中涉及物质变化及焓变
【学习目标】1
知识与技能⑴了解化学反应中能量变化的实质,理解反应热、放热反应、吸热反应等概念
⑵明确测定反应热的要点,测定反应热的基本原理和方法
过程与方法通过化学反应中的能量变化,理解放热反应和吸热反应的实质
且会利用量热计测定反应热
情感态度与价值观通过常见的化学反应的热效应,结合物质的结构,体会化学反应的实质,感受化学反应中的能量变化及能源危机,培养学习化学的兴趣,乐于探究物质变化的奥秘,感受化学世界的奇妙,培养创新精神和实践能力
【学习重难点】1
理解放热反应和吸热反应的实质
课时安排:共2课时教学过程:第一课时【引入新课】从物质结构的角度看,化学反应的实质是旧化学键的断裂和新化学键的生成,因此几乎所有的化学反应都伴随着能量的释放或吸收
通过过去对化学的学习,我们知道在化学反应中,化学能可以与多种形式的能量发生转化,其中最普遍的能量转化是化学能与热能之间的转化
因此可以将化学反应分为放热反应和吸热反应
【板书】第1章化学反应与能量转化第1节化学反应的热效应【投影】【提问】常见的放热反应和吸热反应有哪些类型
【学生】常见的放热反应:①活泼金属与水或酸的反应②酸碱中和反应③燃烧反应④多数化合反应常见的吸热反应:类型比较放热反应吸热反应定义有热量放出的化学反应吸收热量的化学反应形成原因反应物具有的总能量大于生成物具有的总能量反应物具有的总能量小于生成物具有的总能量与化学键强弱关系生成物分子成键时释放出的总能量大于反应物分子断裂旧键时吸收的总能量生成物分子成键时释放出的总能量小于反应物分子断裂旧键时吸收的总能量1反应物所具有的能量生成物所具有的能量①多数分解反