1/9第3课时不同价态含硫物质的转化目标课程标准核心素养1•认识硫兀素在物质中具有不同价态,可以通过氧化还原反应实现不同价态含硫物质的转化
2•能从物质类别和元素价态变化的视角,说明硫及其化合物的转化路径,设计实验进行初步验证,并能分析、解释有关实验现象
1•科学探究与创新意识:能与同伴合作进行实验探究,如实观察、记录实验现象,能根据实验现象形成初步结论
2•科学态度与社会责任:能运用硫及其化合物知识分析讨论生产、生活中简单的化学问题(如环境保护等),认识化学科学对社会可持续发展的贡献
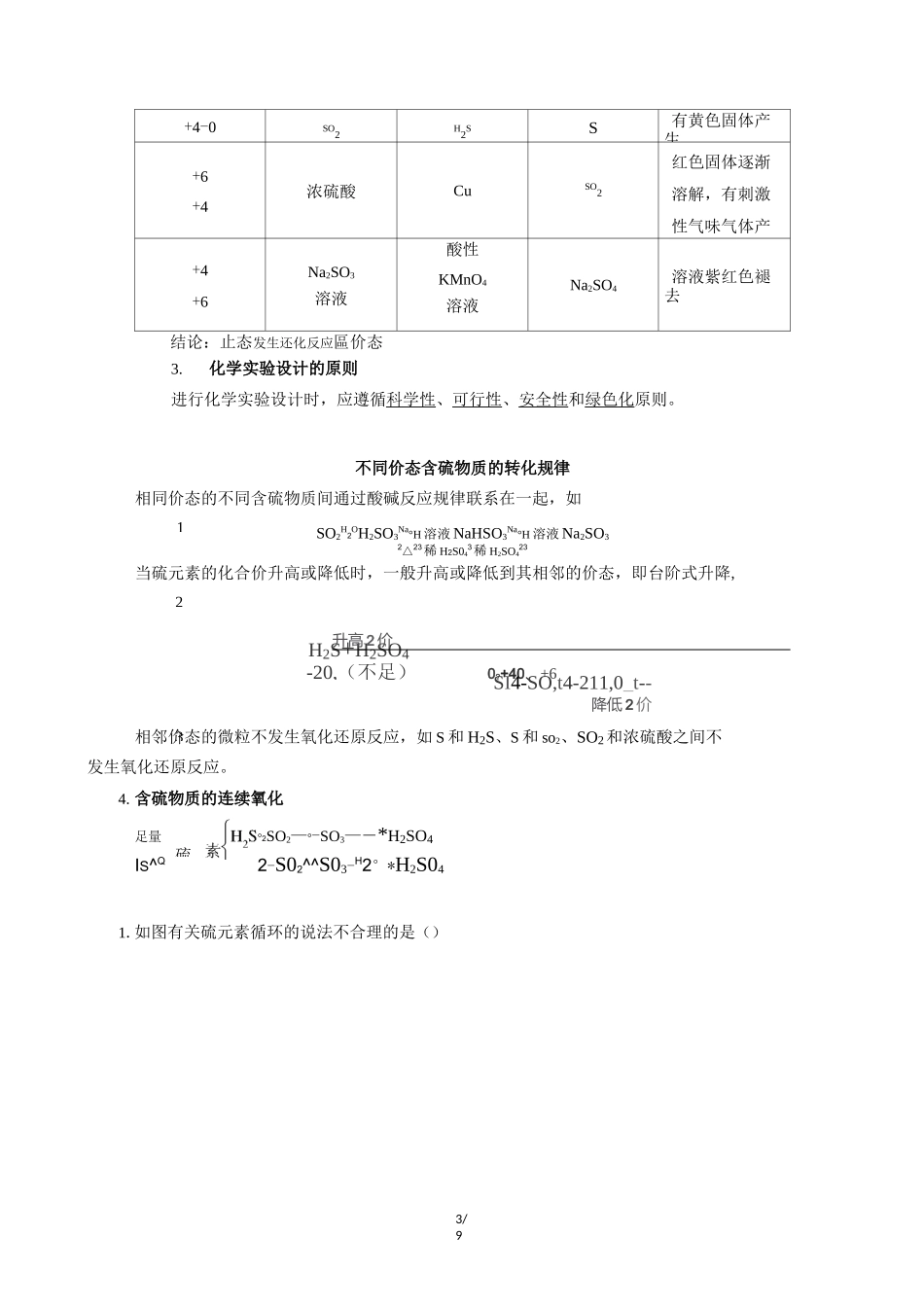
自然界中硫的存在和转化火山喷发喷口附近H2S-S—SO2—SO3H2SO3H2SO4地表附近石膏(CaSO4•2H20)、42芒硝(Na2SO4・10H2O)岩层深处黄铁矿(FeS2)、黄铜矿(CuFeSJ2•实验探究不同价态含硫物质的转化(1)不同价态硫元素的转化与性质(2)实验探究不同价态含硫物质的转化转化目标(价态变化)转化前的含硫物质选择试剂(氧化剂或还原剂)转化后的含硫物质预期现象回扣教材”険圄縊基2/9—2一0Na2S溶液氯水S溶液黄绿色褪去,有黄色沉淀产生0一一2S粉末NaNa2S产生轻微的爆炸声0T4S浓硫酸SO2有刺激性气味体产生3/912-20,(不足)0
+40、+6H2S+H2SO43+4-0SO2H2SS有黄色固体产生+6+4浓硫酸CuSO2红色固体逐渐溶解,有刺激性气味气体产+4+6Na2SO3溶液酸性KMnO4溶液Na2SO4溶液紫红色褪去结论:止态发生还化反应區价态3
化学实验设计的原则进行化学实验设计时,应遵循科学性、可行性、安全性和绿色化原则
不同价态含硫物质的转化规律相同价态的不同含硫物质间通过酸碱反应规律联系在一起,如SO2H2OH2SO3Na°H溶液NaHSO3Na°H溶液Na2SO32△23稀H2S043稀H2SO423当硫元素的化合价升高或降