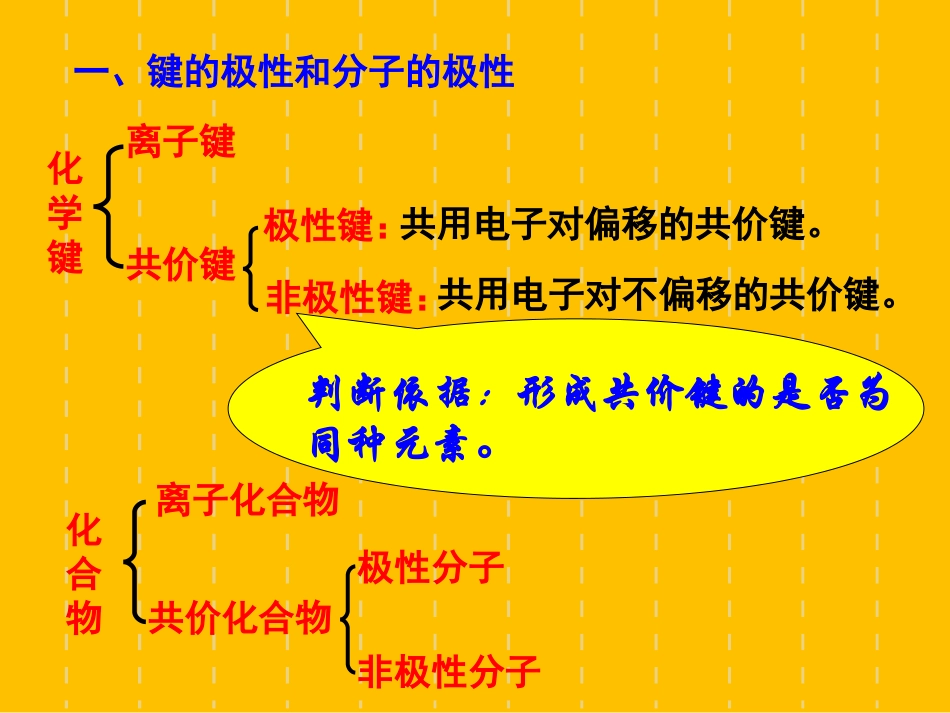
第二章分子结构与性质第二章分子结构与性质第三节第三节《《分子的性质分子的性质》》爱默生告诫我们:爱默生告诫我们:""当一个人年轻时,当一个人年轻时,谁没有空想过?谁没有幻想过?想入非非是谁没有空想过?谁没有幻想过?想入非非是青春的标志。但是,我的青年朋友们,请记青春的标志。但是,我的青年朋友们,请记住,人总归是要长大的。天地如此广阔,世住,人总归是要长大的。天地如此广阔,世界如此美好,等待你们的不仅仅是需要一对界如此美好,等待你们的不仅仅是需要一对幻想的翅膀,更需要一双踏踏实实的脚!幻想的翅膀,更需要一双踏踏实实的脚!"一、键的极性和分子的极性共价键极性键:非极性键:共用电子对偏移的共价键。共用电子对不偏移的共价键。判断依据:形成共价键的是否为同种元素。化学键离子键化合物离子化合物共价化合物极性分子非极性分子极性共价键非极性共价键一、键的极性和分子的极性(一)键的极性HClCl2练习:指出下列微粒中的共价键类型1、O22、CH43、CO24、H2O25、O22-6、OH-非极性键极性键极性键(H-O-O-H)极性键非极性键非极性键极性键极性分子:正电中心和负电中心不重合非极性分子:正电中心和负电中心重合看正电中心和负电中心是否重合(2)化学键的极性的向量和是否等于零(1)看键的极性,也看分子的空间构型2、判断方法:1、概念(二)分子的极性C=O键是极性键,但CO2是直线型分子,两个C=O键是对称排列的,正负电荷中心重合,是非极性分子-OOC-+HOH-O-H键是极性键,共用电子对偏O原子,正负电荷中心不能重合,所以是极性分子++NH3三角锥型,不对称,正负电荷中心不重合,是极性分子-BF3平面三角形,对称,正负电荷中心重合,是非极性分子++---++CH4正四面体型,对称结构,C-H极性键,正负电荷中心重合,是非极性分子CHHHH-++++思考与交流总结:键的极性与分子极性的关系A、都是由非极性键构成的分子一般都是非极性分子。B、极性键结合形成的双原子分子一定为极性分子。C、极性键结合形成的多原子分子,可能为非极性分子,也可能为极性分子。D、多原子分子的极性,应有空间结构,正负电荷中心是否重合共同来决定。共价键极性键非极性键空间不对称极性分子双原子分子:HCl、NO、IBrV型分子:H2O、H2S、SO2三角锥形分子:NH3、PH3非正四面体:CHCl3非极性分子单质分子:Cl2、N2、P4、O2直线形分子:CO2、CS2、C2H2正四面体:CH4、CCl4、CF4空间对称共价键极性和分子极性关系范德华力和氢键范德华力和氢键对物质性质的影响对物质性质的影响思考与交流:判断下列分子中,哪些是极性分子,哪些是非极性分子?H2、O2、P4、CO2、H2O、CH4、Cl2、HCl、C60、HCN、BF3、CH3Cl、NH3我们知道:分子内部原子间存在相互作用——化学键,形成或破坏化学键都伴随着能量变化。物质三相之间的转化也伴随着能量变化。这说明:分子间也存在着相互作用力。二、范德华力及其对物质性质的影响1、范德华力:分子之间的相互作用力,很弱,比化学键小1~2个数量级。只能在很小的范围内存在。不属于化学键分子HClHBrHICOAr范德华力(kj/mol)21.1423.1126.008.758.50共价键键能(kj/mol)431.8366298.7745无2、影响范德华力大小的因素①结构相似的分子,相对分子质量越大,范德华力越大。如卤素单质②分子极性越强,范德华力越大化学键影响物质的化学性质(主)和物理性质范德华力影响物质的物理性质(熔、沸点及溶解度等)分子间范德华力越大,熔沸点越高3、范德华力对物质性质的影响将干冰气化,破坏了CO2分子晶体的—————将CO2气体溶于水,破坏了CO2分子的————分子间作用力共价键思考:练习:下列变化过程只是克服了范德华力的是()A、食盐的熔化B、水的分解C、碘单质的升华D、金属钠的熔化C-150-125-100-75-50-2502550751002345××××CH4SiH4GeH4SnH4NH3PH3AsH3SbH3HFHClHBrHIH2OH2SH2SeH2Te沸点/℃周期一些氢化物的沸点1.定义:是由已经与电负性很强的原子形成共价键的氢原子(如水分子中的氢)与另一个分子中电负性很强的原子(如水分子中的氧)之间的作用力这种相互作用称氢键。三、氢键及其对物质性质的影响22..表示表示:氢键可以用:氢键可以用X—HX—H...