高一化学概念原理教案教学目标:知识和技能:1
复习离子反应和氧化还原反应的有关概念2
复习物质的量应用于化学方程式的计算
过程与方法:初步学会从氧化还原反应的视角研究物质的化学性质的方法,学会自己分析、归类、总结的复习方法;情感态度价值观:通过交流、讨论,加强学生之间的合作学习;能从环保角度评价实验方案;教学重点:氧化还原思想在元素化合物学习中的应用
教学难点:引入氧化还原反应概念的意义教学过程:教师活动学生活动设计意图回想AgNO3溶液与NaCl溶液混合、向CuCl2溶液加铁钉的实验现象引导学生分析反应的本质描述实验现象,写出反应方程式思考,可能回答::从反应本质分析是离子反应;第2个还有电子的转移
写出离子反应方程式用初中熟悉的反应引入,引起学生对反应由表象向本质的分析
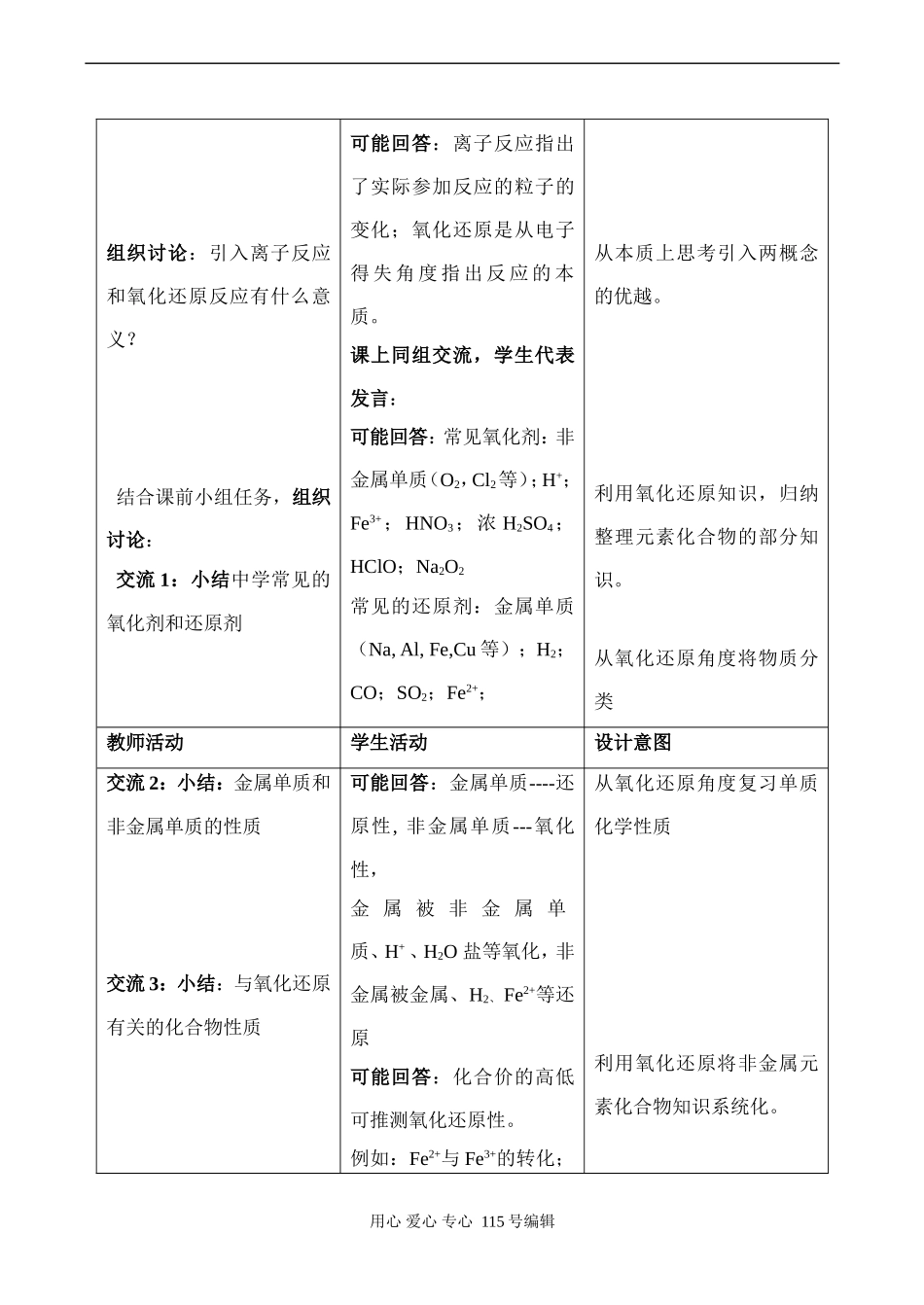
用心爱心专心115号编辑组织讨论:引入离子反应和氧化还原反应有什么意义
结合课前小组任务,组织讨论:交流1:小结中学常见的氧化剂和还原剂可能回答:离子反应指出了实际参加反应的粒子的变化;氧化还原是从电子得失角度指出反应的本质
课上同组交流,学生代表发言:可能回答:常见氧化剂:非金属单质(O2,Cl2等);H+;Fe3+;HNO3;浓H2SO4;HClO;Na2O2常见的还原剂:金属单质(Na,Al,Fe,Cu等);H2;CO;SO2;Fe2+;从本质上思考引入两概念的优越
利用氧化还原知识,归纳整理元素化合物的部分知识
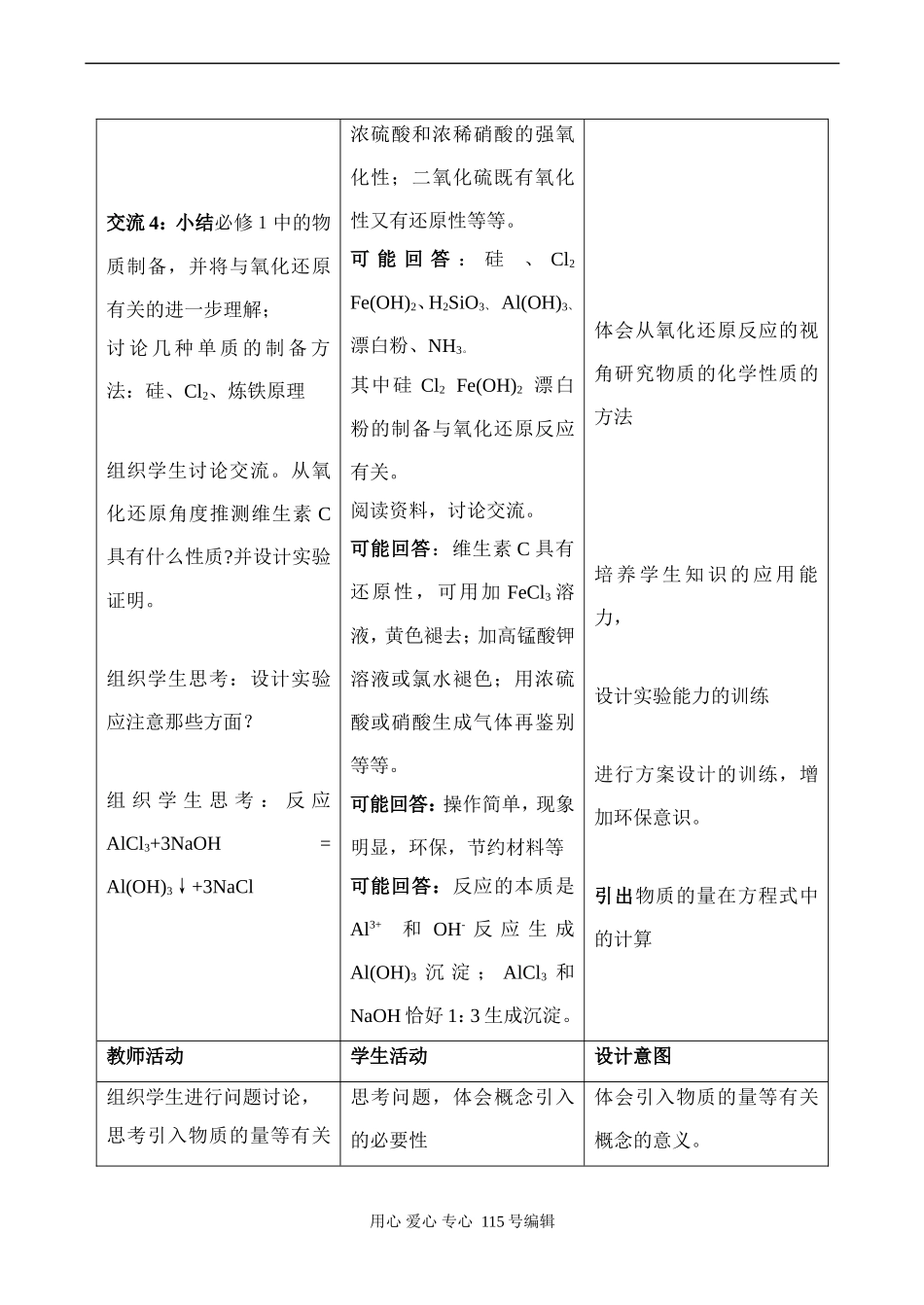
从氧化还原角度将物质分类教师活动学生活动设计意图交流2:小结:金属单质和非金属单质的性质交流3:小结:与氧化还原有关的化合物性质可能回答:金属单质----还原性,非金属单质---氧化性,金属被非金属单质、H+、H2O盐等氧化,非金属被金属、H2、Fe2+等还原可能回答:化合价的高低可推测氧化还原性
例如:Fe2+与Fe3+的转化;从氧化还原角度复习单质化学性质利用氧化还原将非金属元素化合