分子的立体结构第二课时[复习]共价键类型:σ、π键,价层电子对互斥模型
[质疑]我们已经知道,甲烷分子呈正四面体形结构,它的4个C--H键的键长相同,H—C--H的键角为109~28°
按照我们已经学过的价键理论,甲烷的4个C--H单键都应该是π键,然而,碳原子的4个价层原子轨道是3个相互垂直的2p轨道和1个球形的2s轨道,用它们跟4个氢原子的ls原子轨道重叠,不可能得到四面体构型的甲烷分子
[板书]三、杂化轨道理论简介[讲解]杂化轨道理论是一种价键理论,是鲍林为了解释分子的立体结构提出的
为了解决甲烷分子四面体构型,鲍林提出了杂化轨道理论,它的要点是:当碳原子与4个氢原子形成甲烷分子时,碳原子的2s轨道和3个2p轨道会发生混杂,混杂时保持轨道总数不变,却得到4个相同的轨道,夹角109°28′,称为sp3杂化轨道,表示这4个轨道是由1个s轨道和3个p轨道杂化形成的
当碳原子跟4个氢原子结合时,碳原子以4个sp3杂化轨道分别与4个氢原子的ls轨道重叠,形成4个C--Hσ键,因此呈正四面体的分子构型
[投影]sp3杂化轨道[板书]1、sp3杂化:1个s轨道和3个p轨道会发生混杂,得到4个相同的轨道,夹角109°28′,称为sp3杂化轨道
[讲解]价层电子对互斥模型时我们知道,H20和NH3的VSEPR模型跟甲烷分子一样,也是四面体形的,因此它们的中心原子也是采取sp3杂化的
所不同的是,水分子的氧原子的sp3杂化轨道有2个是由孤对电子占据的,而氨分子的氮原子的sp3杂化轨道有1个由孤对电子占据[板书]空间结构:空间正四面体或V型、三角锥型
[讲解]除sp3杂化轨道外,还有sp杂化轨道和sp2杂化轨道
sp杂化轨道由1个s轨道和1个p轨道杂化而得;sp2杂化轨道由1个s轨道和2个p轨道杂化而得
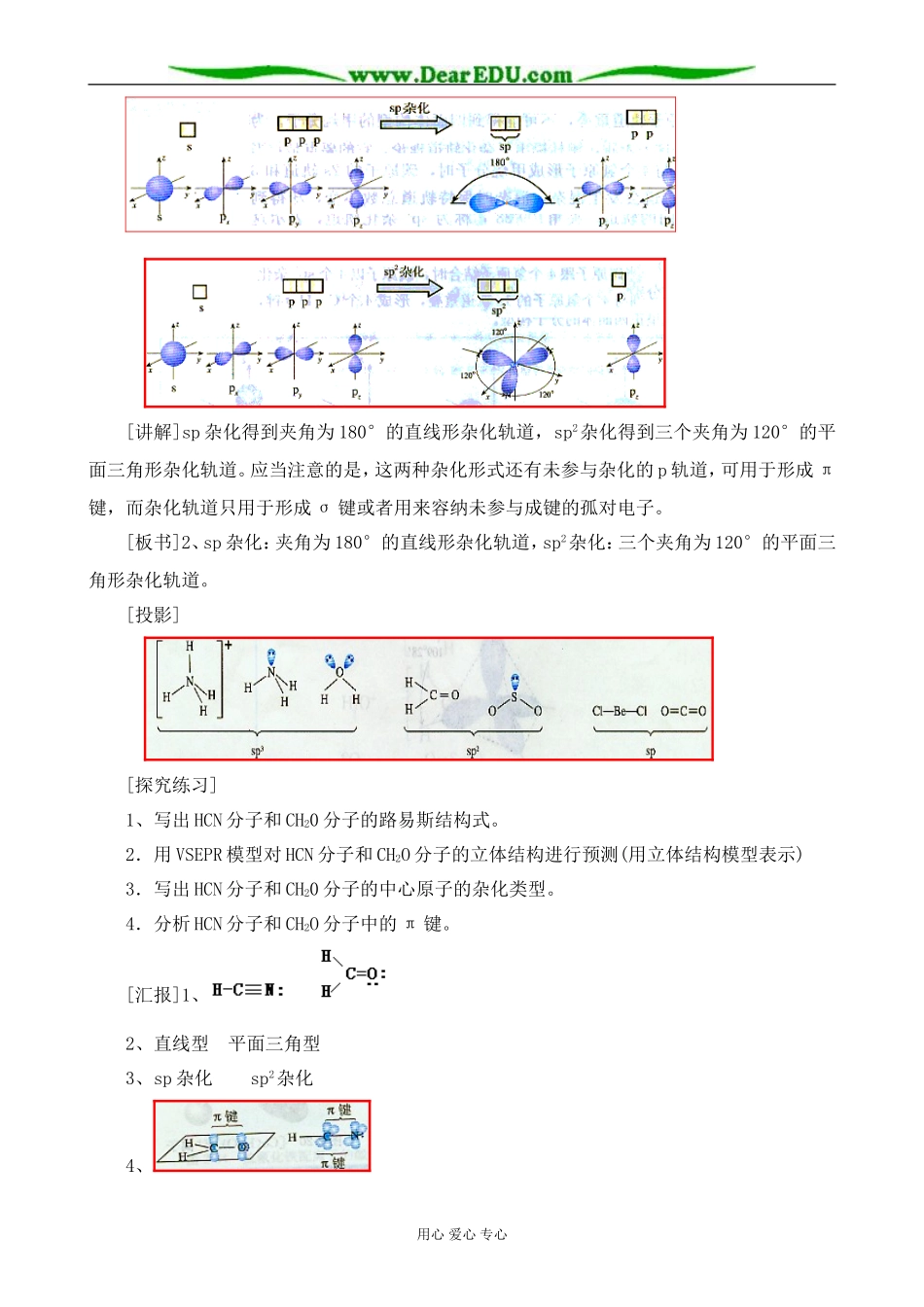
[投影]用心爱心专心[讲解]sp杂化得到夹角为180°的直线形杂化轨道,sp2