食品中大肠菌群MPN计数法测定操作规程1目的对公司产品的大肠菌群测定制定标准操作规程,保证公司大肠菌群(MPN法)检测的规范性和检测结果的准确性
2范围本操作规范适用于颐海国际控股有限公司、食品类大肠菌群标准单位为MPN的产品
3依据GB4789
3-2016《食品安全国家标准食品微生物学检验大肠菌群计数》第一法大肠菌群MPN计数法、GB4789
3-2003《食品安全国家标准食品微生物学检验大肠菌群计数》
4实验原理MPN法是统计学和微生物学结合的一种定量检测法
待测样品经系列稀释并培养后根据其未生长的最低稀释度与生长的最高稀释度,应用统计学概率论推算出待测样品中大肠菌群的最大可能数
5仪器和设备微生物实验室常规灭菌及培养设备外,其他设备和材料如下:5
1恒温培养箱:36°C±1°C5
2冰箱:2C-5C5
4天平:感量0
6无菌吸管:1mL、10mL(具0
1mL刻度)及吸头6
培养基和试剂6
1月桂基硫酸盐胰蛋白胨肉汤(LST)、煌绿乳糖胆盐肉汤(BGLB)、乳糖胆盐发酵培养基、伊红美蓝琼脂、乳糖发酵培养基、1mol//LNaOH、1mol/LHCl
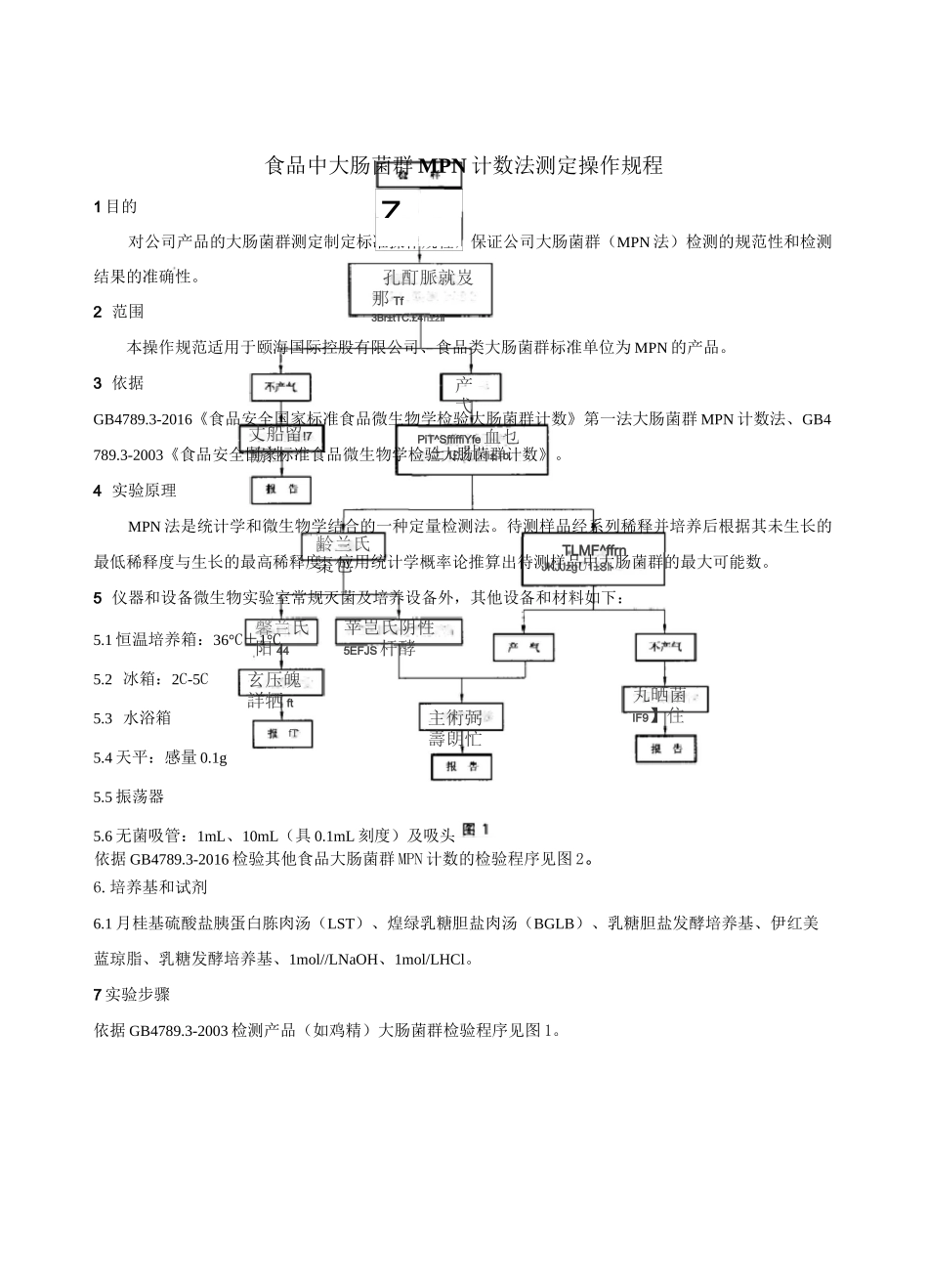
7实验步骤依据GB4789
3-2003检测产品(如鸡精)大肠菌群检验程序见图1
fT产弋馨兰氏阳44玄压魄詳牺ft丸晒菌IF9】住PiT^SffiffiYfe血乜±1£
肚ti±1bTLMF^ffrnJKJJzgU1±Sli苹岂氏阴性5EFJS杆酵丈船留
7協性齢兰氏棗包主術弼壽朗忙依据GB4789
3-2016检验其他食品大肠菌群MPN计数的检验程序见图2
Z孔酊脈就岌那Tf3Br±tTC
£4h±2li图27
1样品的稀释7
1固体和半固体样品:称取25g样品,放入盛有225ml的生理盐水的无菌均质盒内,充分混匀制成1:10的样品匀液
2液体样品:以无菌吸管吸取25ml样