第10讲弱电解质的电离平衡(1)第一页,共二十九页
考纲要求2011考纲展示2012高考导视1
了解电解质、强电解质及弱电解质的概念
了解电解质在水溶液中的电离,以及电解质溶液的导电性
了解弱电解质在水溶液中的电离平衡
了解水的电离、离子积常数
了解溶液pH的定义,掌握测定溶液pH的方法,能进行pH的简单计算
掌握强电解质、弱电解质等基本概念
溶液的导电性、弱酸的酸性相对强弱比较、电离常数的计算、水的电离平衡、pH的计算、中和滴定等是重要的考点
离子浓度大小比较、离子守恒关系是高频考点
第二页,共二十九页
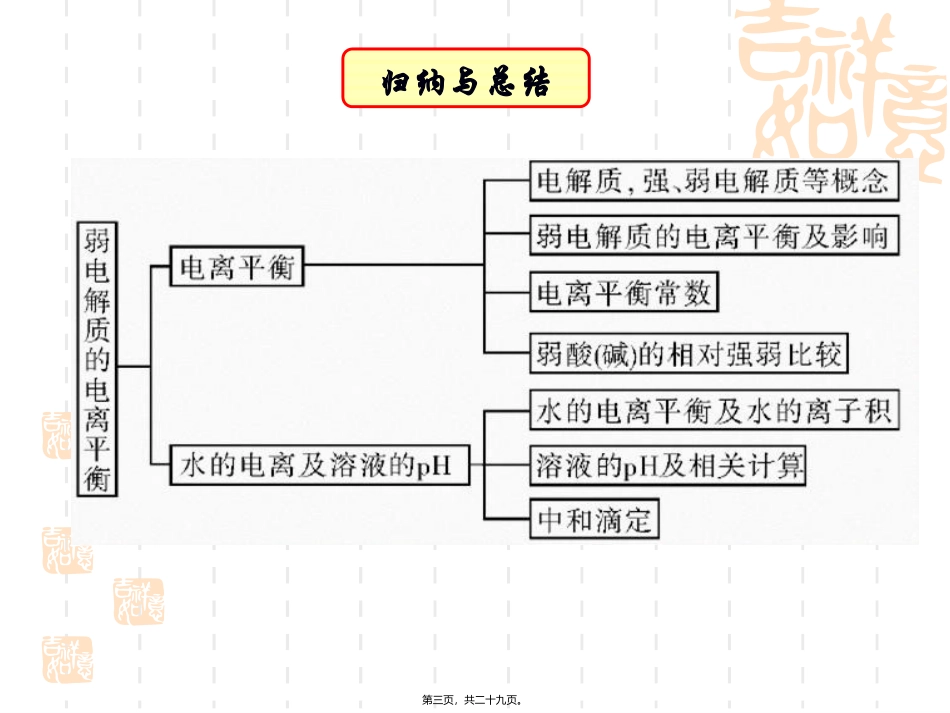
归纳与总结第三页,共二十九页
一、强电解质和弱电解质1.概念(1)强电解质:在水溶液里能够的电解质,主要包括、、等
(2)弱电解质:在水溶液里的电解质,主要包括、和少部分盐及水等
全部电离强酸强碱大多数盐部分电离弱酸弱碱想一想:常见的强酸、强碱有哪些
哪些盐是弱电解质
基础知识梳理第四页,共二十九页
2.电离方程式的书写(1)强电解质电离用“”号,弱电解质电离用“”号
(2)多元弱酸分步电离,且第一步电离程度远远大于第二步,如H2CO3的电离方程式为:,
(3)多元弱碱电离方程式一步写成,如Fe(OH)3的电离方程式为:
知识点1===第五页,共二十九页
强电解质弱电解质①结构:离子键或强极性键;②电离程度:在水溶液中完全电离(溶液中只有离子存在而无电解质分子存在);③电离过程:不存在电离平衡,即电离过程不可逆
用“=”表示电离过程
④溶液中微粒:水合离子①结构:“弱”极性键②电离程度:在水溶液中部分电离,溶液中既有离子又有电解质分子存在;③电离过程:有电离平衡存在,即电离过程可逆
用“”表示电离过程
④溶液中微粒:分子、水合离子范围:强酸(如HCl、HBr、HI、HNO3、H2SO4、HClO4等酸)、强碱、绝大多数盐弱酸、弱碱、水、某些