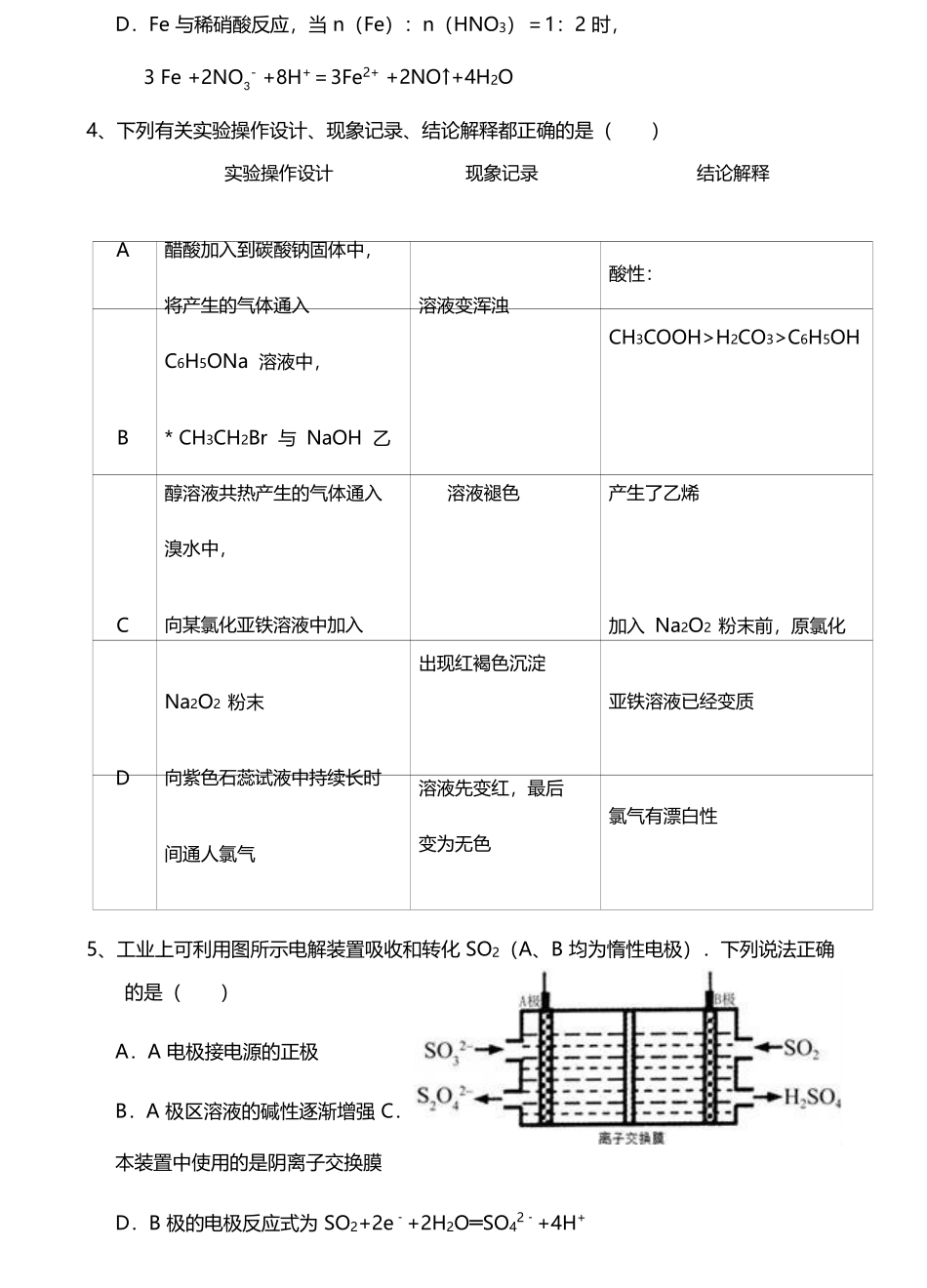
天津一中2016-2017五月考理综化学部分理科综合化学部分第Ⅰ卷以下数据可供解题时参考:相对原子质量:H1O16C12N14Na23Cl35.5Cr521、下列说法正确的是()A.向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成B.Na、Mg、Fe等金属在一定条件下与水反应都生成H2和对应的碱C.同主族元素的简单阴离子还原性越强,水解程度越大D.符合通式CnH2n+2的不同烃不一定互为同系物2、用NA表示阿伏加德罗常数的值,下列说法正确的是()A.1mol·L-1AlCl3溶液中,含Al3+数目小于NAB.标准状况下,6.0gNO和2.24LO2混合,所得气体的分子数目为0.2NAC.25℃,1LpH=1的稀硫酸中含有的H+数为0.2NAD.由1molCH3COONa和少量CH3COOH形成的中性溶液中,CH3COOˉ数目为NA个3、下列离子方程式书写不正确的是()A.AlCl3溶液与烧碱溶液反应,当n(OH-):n(Al3+)=7:2时,2Al3++7OH-=Al(OH)3↓+AlO2-+2H2OB.CuCl2溶液与NaHS溶液反应,当n(CuCl2):n(NaHS)=1:2时Cu2++2HS-=CuS↓+H2S↑C.Cl2与FeBr2溶液反应,当n(Cl2):n(FeBr2)=1:1时,2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-3实验操作设计现象记录结论解释A醋酸加入到碳酸钠固体中,酸性:将产生的气体通入溶液变浑浊CH3COOH>H2CO3>C6H5OHC6H5ONa溶液中,B*CH3CH2Br与NaOH乙醇溶液共热产生的气体通入溶液褪色产生了乙烯溴水中,C向某氯化亚铁溶液中加入加入Na2O2粉末前,原氯化出现红褐色沉淀Na2O2粉末亚铁溶液已经变质D向紫色石蕊试液中持续长时溶液先变红,最后氯气有漂白性变为无色间通人氯气D.Fe与稀硝酸反应,当n(Fe):n(HNO3)=1:2时,3Fe+2NO-+8H+=3Fe2++2NO↑+4H2O4、下列有关实验操作设计、现象记录、结论解释都正确的是()5、工业上可利用图所示电解装置吸收和转化SO2(A、B均为惰性电极).下列说法正确的是()A.A电极接电源的正极B.A极区溶液的碱性逐渐增强C.本装置中使用的是阴离子交换膜D.B极的电极反应式为SO2+2e﹣+2H2O═SO42﹣+4H+6、其他条件不变时,改变密闭容器中某一条件,对反应A2(g)+3B2(g)2AB3(g)化学平衡状态的影响,得到如右图所示的曲线(T表示温度,n表示物质的量)。下列判断正确的是A.若T1>T2,则正反应是吸热反应B.达到平衡时,A2转化率:b>a>cC.在T2和起始n(A2)不变时达到平衡,n(AB3)大小为:c>b>aD.若T2>T1,达到平衡时b、d两点的反应速率为:d>b第Ⅱ卷7.(14分)原子序数由小到大排列的四种短周期元素X、Y、Z、W的原子序数之和为32,在元素周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族,且Z为地壳中含量最多的元素。M元素与X同主族,与W同周期。(1)M元素在周期表中位置为。(2)Z、W形成的气态氢化物的稳定性为>。(填化学式)(3)气态Y2X4是一种常见燃料,可与YZ2反应,每转移1mol电子且生成气态X2Z放出142KJ热量,写出有关热化学方程式。(4)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为。(5)由X、Y、Z、W四种元素组成的一种离子化合物A,已知①1molA能与足量NaOH浓溶液反应生成标准状况下44.8L气体。②A能与盐酸反应产生气体B,该气体能与氯水反应。则A是(填化学式)。写出该气体B与氯水反应的离子方程式。(6)由X、Y、Z、W和Fe五种元素组成的相对分子质量为392的化合物C,1molC中含有6mol结晶水。对化合物C进行如下实验:a.取C的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;b.另取C的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。①C水溶液中各种离子浓度由大到小的顺序为:。②试写出C与M2Z2按物质的量之比为1∶2在溶液中反应的化学方程式。8.(18分)新泽茉莉醛是一种名贵的香料,合成过程中还能得到一种PC树脂,其合成路线如下。(1)E的含氧官能团名称是,E分子中共面原子数目最多为。(2)写出反应①的化学方程式。(3)写出符合下列条件并与化合物E互为同分异构体的有机物结构简式。a.能与浓溴水产生白色沉淀b.能与NaHCO3溶液反应产生气体c.苯环上一氯代物有两种(4)反应②的反应类型是。(5)已知甲的相对分子质量为30,写出甲和G...