氨肥的生产和使用氨肥的生产和使用氨气一一
氨气的物理性质氨气的物理性质3
极易液化,液氨汽化时要吸收大量热1
无色,有特殊刺激性气味的气体2
常温常压下,1V水约能溶解700V氨气4
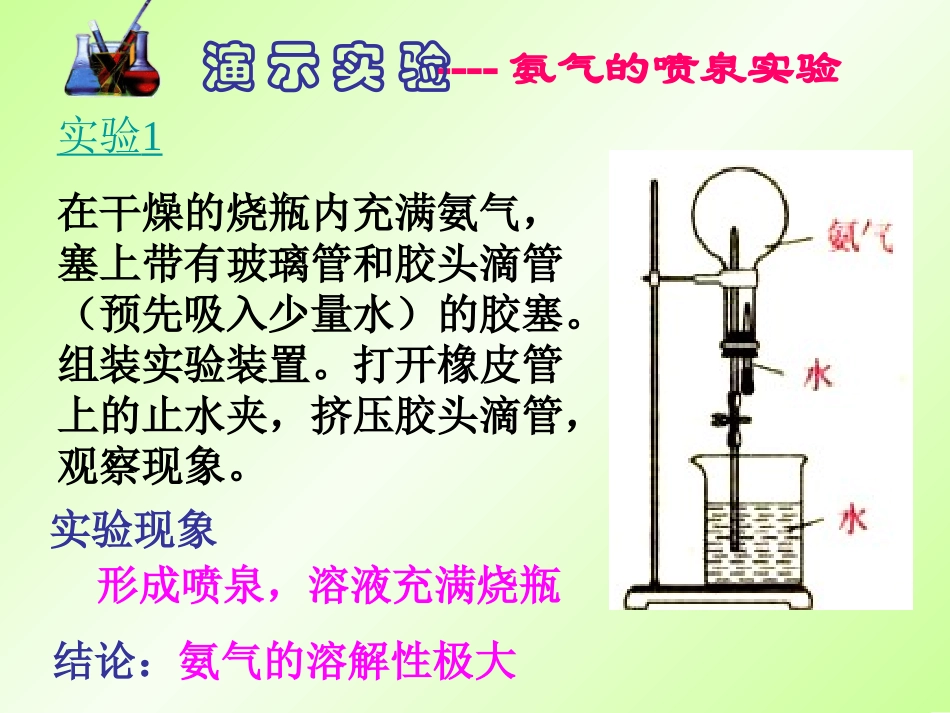
氨水密度比水小实验1在干燥的烧瓶内充满氨气,塞上带有玻璃管和胶头滴管(预先吸入少量水)的胶塞
组装实验装置
打开橡皮管上的止水夹,挤压胶头滴管,观察现象
实验现象形成喷泉,溶液充满烧瓶结论:氨气的溶解性极大----氨气的喷泉实验演示实验----氨气的喷泉实验演示实验(2)溶液为什么变为红色
(3)实验成败的关键是什么
(1)氨为什么会形成喷泉
烧瓶干燥;b
装置的气密性好;c
收集的气体纯度尽可能高
氨气溶于水溶液显碱性
氨极易溶于水,使烧瓶内外形成较大的压差;城市中常见的人造喷泉及火山爆发的原理与上述的原理相似吗
氨气的化学性质氨气的化学性质1
与水反应与水反应NHNH33是唯一能使红色石蕊试纸变蓝的气体是唯一能使红色石蕊试纸变蓝的气体NHNH33+H+H22ONHONH33·H·H22OONHNH44+++OH+OH--2
与酸的反应与酸的反应NH3+HCl==NH4Cl现象:冒白烟现象:冒白烟(常用硫酸作为氨气的吸收剂)(常用硫酸作为氨气的吸收剂)原因:是原因:是NHNH44ClCl的固体微小晶体悬浮在空中的固体微小晶体悬浮在空中NH3+HNO3=NH4NO42NH3+H2SO4=(NH4)2SO4此外:此外:NH3+H+=NH4+3
与氧气反应与氧气反应4NH4NH33+5O+5O22====4NO+6H====4NO+6H22OO催化剂表现出表现出NHNH33的还原性的还原性氨的催化氧化(工业制硝酸的第一步)氨的催化氧化(工业制硝酸的第一步)2NH3+3Cl2==N2+6HCl(氨不足)8NH3+3Cl2==N2+6NH4Cl(氨充足)四、氨气的