实验二螺旋位错生长过程观察一、实验目的1
了解水溶液中的溶解度与结晶原理;2
认识枝晶生长的基本过程;3
观察晶体生长的螺旋位错,计算台阶横向生长速率及其与驱动力的关系
观察手性晶体
二、实验设备及材料1、带CCD的显微镜;2、载玻片;3、盖玻片;4、偏光片;5、加热装置;6、碘化镉;7、氯酸钠;8、有机晶体(Phenylsalicylate,对羟基苯甲酸苯酯,HOC6H4COOC6H5,熔点:42-44oC);9、去离子水;10、药勺;11、烧杯;12、玻璃棒;13、滴管;14、培养皿;15、量筒;16、投影仪
三、实验原理(1)溶解度一定的温度下,在一定量的水中,所能溶解的溶质量是有限的,常用溶解度来表示
溶解度指的是,在一定温度下,某固态物质在100g水中达到饱和状态时所溶解的质量
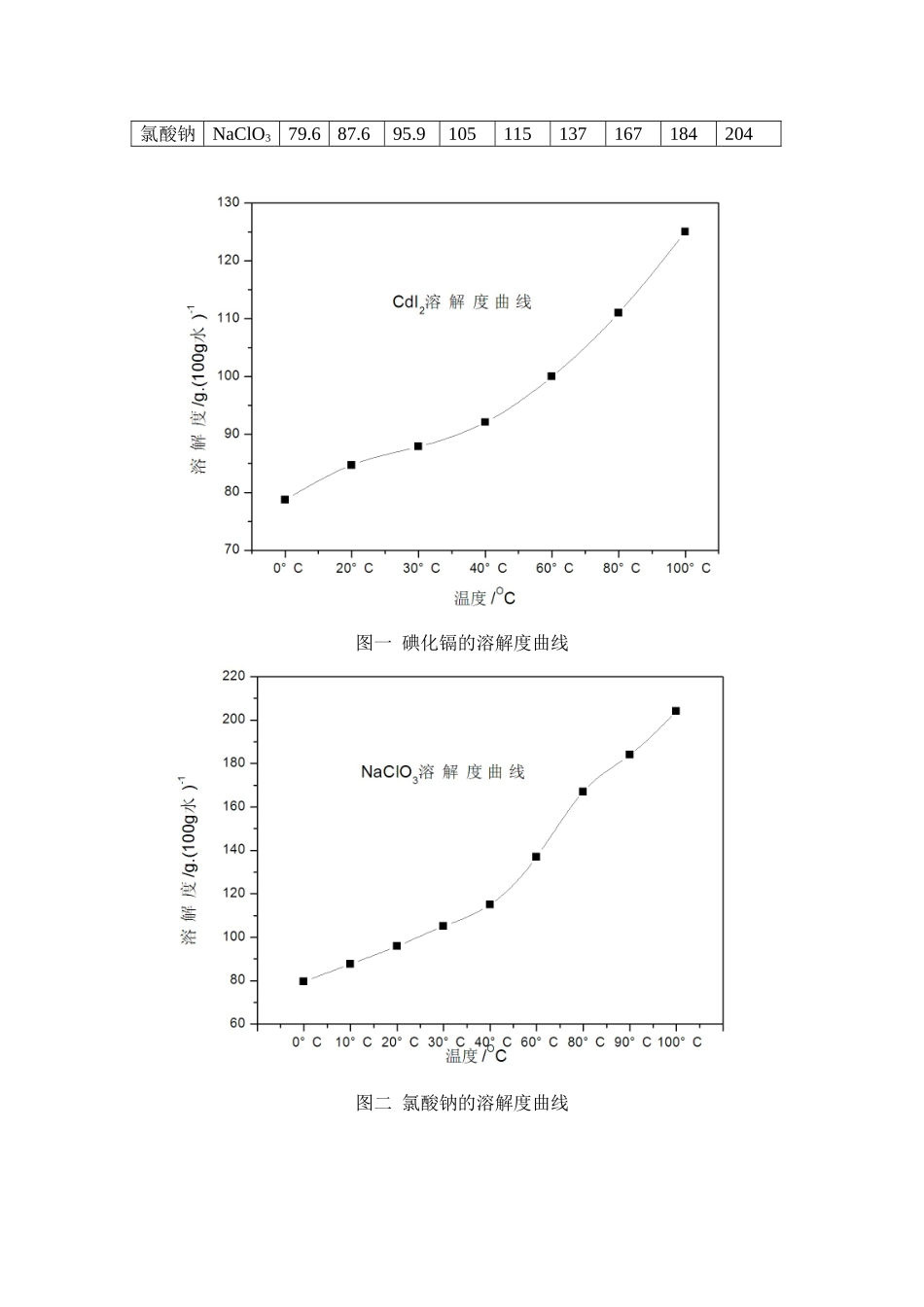
图一和图二分别是碘化镉和氯酸钠的溶解度曲线(数据见表一和表二)
大多数固体物质的溶解度随温度的升高而增大
因此利用较高温度配置溶液达到饱和后,再降低温度,水溶液在高温中溶解度较高,一旦降温后,溶解度也降低,但溶质的量不减,因此,水溶液的浓度大于最大溶解度,此时的溶液成为“过饱和溶液”
过饱和溶液是一种不稳定状态,过量的溶质会结晶析出而成为饱和溶液
常利用此种方法进行结晶提纯
另外随着溶剂水分的蒸发,饱和溶液浓度逐渐变浓而达到饱和,继而也会开始结晶
降温和溶剂蒸发是晶体结晶的两种最主要的方式
表一不同温度下碘化镉的溶解度物质化学式0°C20°C30°C40°C60°C80°C100°C碘化镉CdI278
1100111125表二不同温度下氯酸钠的溶解度物质化学式0°C10°C20°C30°C40°C60°C80°C90°C100°C氯酸钠NaClO379
9105115137167184204图一碘化镉的溶解度曲线图二氯酸钠的溶解度曲线(2)晶体生