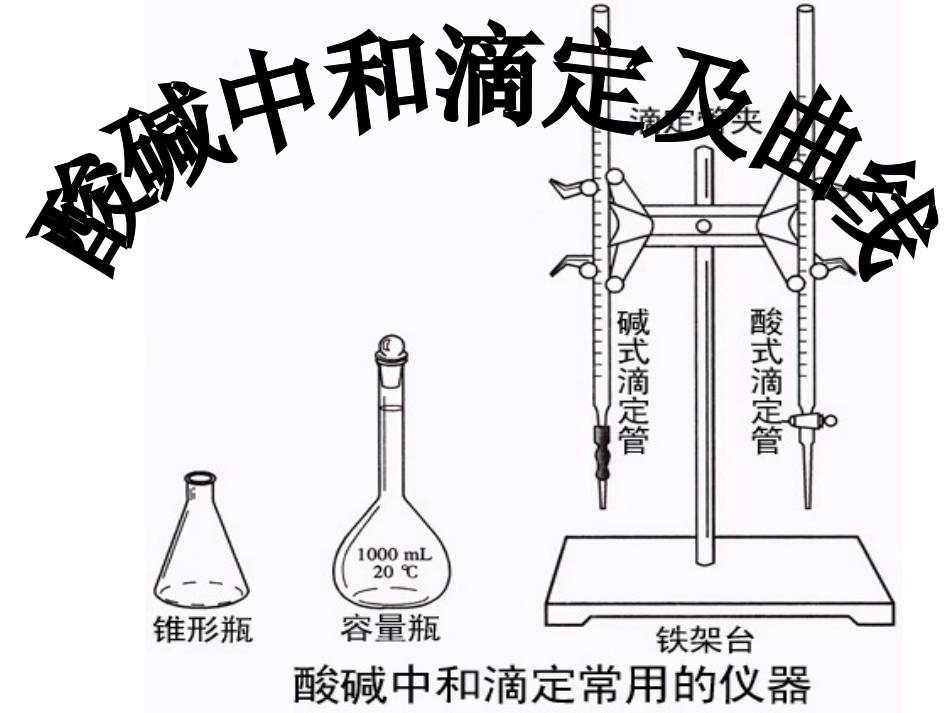
1、酸式滴定管和碱式滴定管的区别和使用方法注意:酸式滴定管不能用于装碱性溶液,碱式滴定管不能用于装酸性溶液或会腐蚀橡胶的溶液(如强氧化性的溶液)
玻璃活塞橡胶管玻璃球2、滴定管的刻度特点和读数方法0刻度处25ml刻度处①0刻度在上方②精密度:0
01ml,所以读数时要读到小数点后两位
③实际滴出的溶液体积=滴定后的读数-滴定前的读数练习:读出以下液体体积的读数78滴定管87量筒25ml酸式滴定管滴定管的构造①上端标有:、、;温度0刻度容积25℃25mL50mL全部盛满溶液时,体积所标容积
多于下端②滴定管的最小刻度为,允许估计至,因此读数的精确度为mL
01酸碱中和滴定正确视线仰视视线正确读数仰视读数读数偏大正确视线俯视视线正确读数俯视读数读数偏小一、定义一、定义用已知浓度用已知浓度的酸的酸((或碱或碱))来来测测定定未知浓度未知浓度的碱的碱((或酸或酸))浓度的实验方法浓度的实验方法叫做酸碱中和滴定
叫做酸碱中和滴定
–已知浓度的溶液——标准液–未知浓度的溶液——待测液二、原理酸HmR和碱M(OH)n反应,当恰好完全反应时,酸提供的H+的物质的量等于碱提供的OH-的物质的量,即:C(C(酸酸)·V()·V(酸酸):C():C(碱碱)·V()·V(碱碱)==n:m)==n:m,或,或者者C(C(酸酸))··V(V(酸酸))··m=C(m=C(碱碱))··V(V(碱碱))··nn中和反应的实质中和反应的实质n(Hn(H++)=n(OH)=n(OH--))H++OH-=H2OnHmR+mM(OH)n=MmRn+mnH2O酸碱中和反应有关量的关系和计算
•[例题]有未知浓度的氢氧化钠溶液0
23L,需加入0
11mol/L的盐酸溶液0
29L,氢氧化钠溶液的物质的量浓度是多少
已知V碱=0
23L,V酸=0
29L,c酸=0
11mol/L求:c碱=