离子一:教学目标1.知道原子核外电子是分层排布的
(难点)2.了解离子的形成,初步认识离子是构成物质的一种粒子
(重点)3.了解原子结构示意图涵义及原子最外层电子数与元素性质的关系
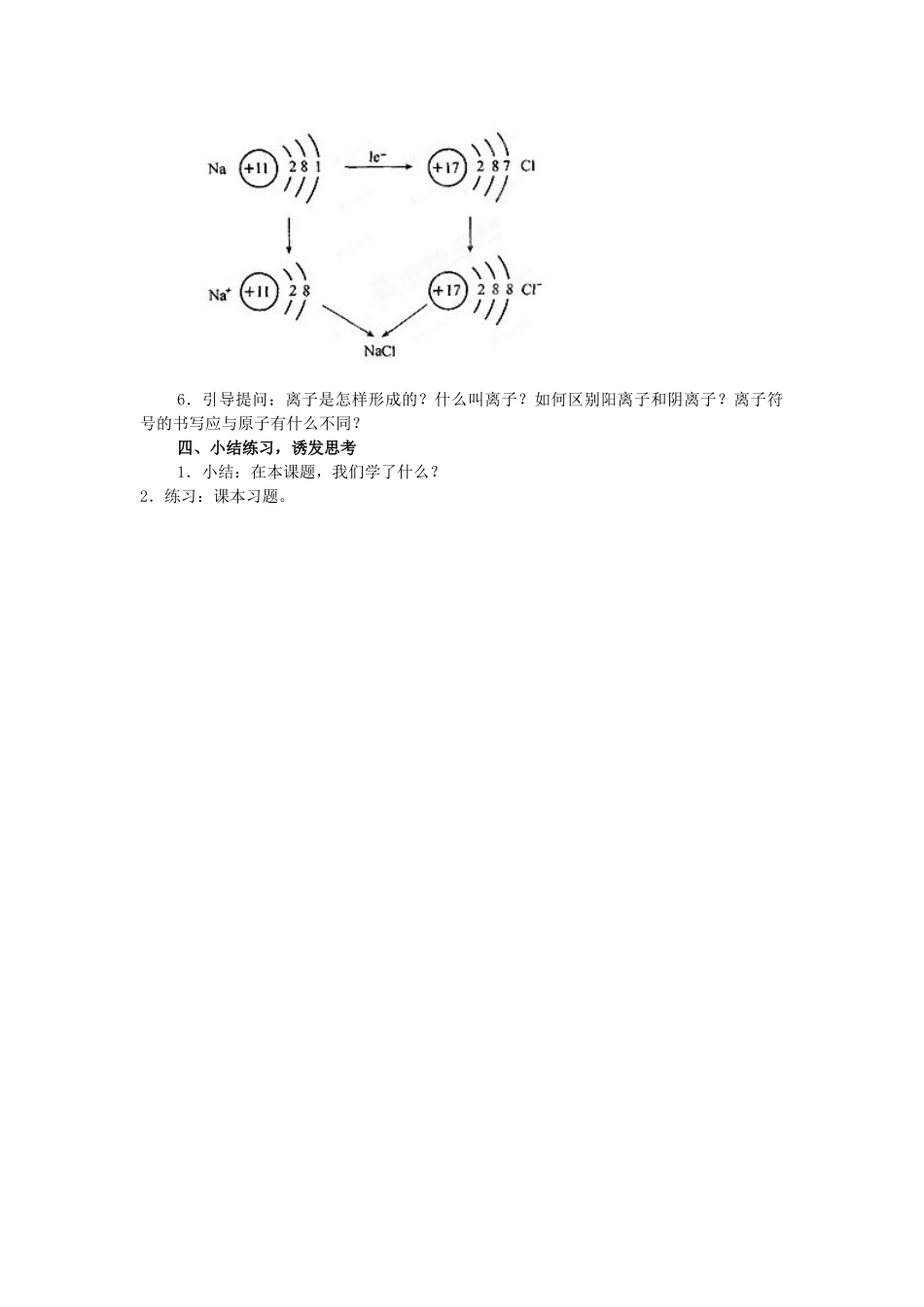
4.探究分析NaCl的形成过程,了解离子的形成,初步认识离子是构成物质的一种粒子
二:教材分析重点:离子的形成难点:核外电子的排布三:教学过程一、情境导入1.学生富有感情地朗读作品──科普小论文《漫游原子世界》,巩固原子结构的知识
附文:我是一个小小的电子,我在原子里围绕着原子核不停地转动,虽然空间很大,但我和我的同伴总想挣脱原子核的吸引
可是原子核这个小老头很有能耐,虽然只占原子的一丁点空间,里面却由质子和中子构成,中子不带电,质子带正电,正好把我身上的负电深深吸引
2.设问:原子核外电子是如何运动的呢
它们能否挣脱原子核的吸引呢
二、引导探究核外电子的排布1学生猜想:核外电子是如何运动的
2.学生交流:向你的同学说一说你想象中核外电子如何运动
3.探究证明假设:阅读课本图文
4.归纳结论:核外电子是分层排布的
5.教师启发:科学家在探索原子核外电子运动时,也经历了假设、猜想的阶段,然后通过科学的手段、借助先进的仪器进行实验测定、检验而得到真理的
那么电子为什么有的排在第一层
有的排在第二层
各电子层上电子数目有什么规律
(让学生体验科学探究的过程后,进一步启发学生对电子排布的想象,提醒学生到高中后还会有更深入的研究,有兴趣的同学可自己查阅有关资料)6.学习原子结构示意图表示的意义:7.练习巩固:向你的同桌说一说下列原子结构示意图的意义:8.展示挂图:1~18号元素的原子结构示意图
学生观察、互相讨论、归纳原子最外层电子数目与元素性质的关系:元素最外层电子数元素化学性质稀有气体元素8个(He为2)比较稳定金属元素少于4个不稳定非金属元素多于4个不稳定9.教师设问:稀有气体元素原子最外层电子数为