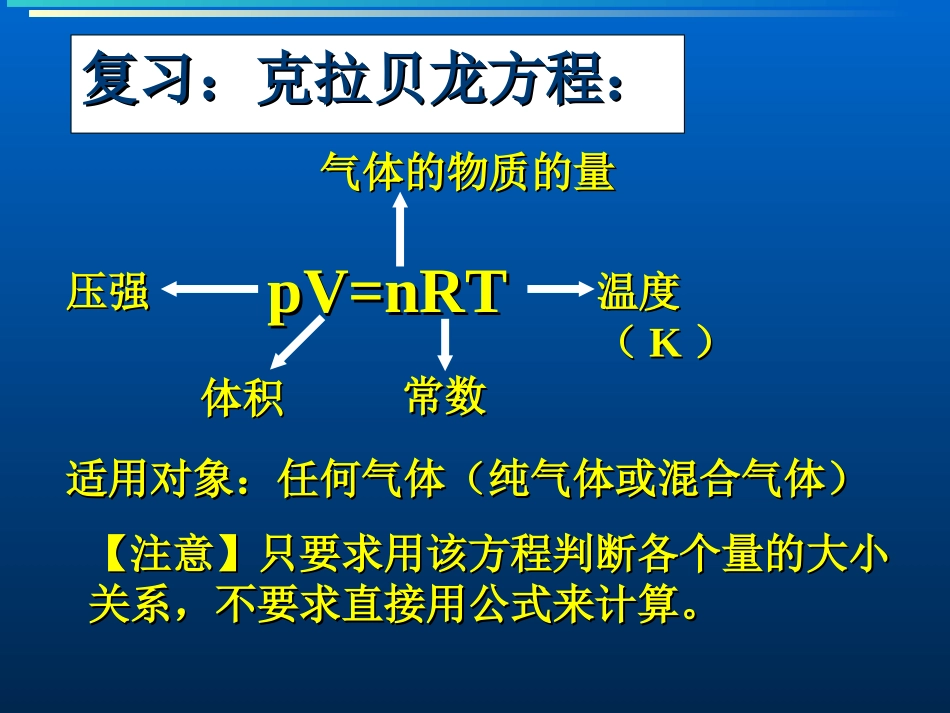
混合气体的相对分子质量混合气体的相对分子质量的计算方法的计算方法复习:克拉贝龙方程:复习:克拉贝龙方程:适用对象:任何气体(纯气体或混合气体)适用对象:任何气体(纯气体或混合气体)pV=nRTpV=nRT压强压强体积体积气体的物质的量气体的物质的量常数常数温度温度((KK))【注意】只要求用该方程判断各个量的大小【注意】只要求用该方程判断各个量的大小关系,不要求直接用公式来计算。关系,不要求直接用公式来计算。(三)阿伏加德罗定律的推论:(三)阿伏加德罗定律的推论:依据:依据:pV=nRTpV=nRT或或pV=pV=RTMm1.1.同温同压下,任何气体体积之比等同温同压下,任何气体体积之比等于于((TT、、pp相同)相同)212121NNnnVV物质的量之比物质的量之比(三)阿伏加德罗定律的推论:(三)阿伏加德罗定律的推论:依据:依据:pV=nRTpV=nRT或或pV=pV=RTMm2.2.同温同压下,任何气体密度比等于同温同压下,任何气体密度比等于((TT、、pp相同)相同)相对2121MM相对分子质量之比(摩尔质量之比)相对分子质量之比(摩尔质量之比)(三)阿伏加德罗定律的推论(三)阿伏加德罗定律的推论依据:依据:pV=nRTpV=nRT或或pV=pV=RTMm2121mmMM((TT、、pp、、VV相同)相同)3.3.同温同压下,相同体积任何气体的同温同压下,相同体积任何气体的质量比等于质量比等于相对分子质量之比相对分子质量之比(三)阿伏加德罗定律的推论:(三)阿伏加德罗定律的推论:依据:依据:pV=nRTpV=nRT或或pV=pV=RTMm4.4.同温同体积下,任何气体的压强之比同温同体积下,任何气体的压强之比等于等于((TT、、VV相同)相同)212121NNnnpp物质的量之比物质的量之比12/29/2412/29/2412/29/24(四)气体的相对分子质量的计算方法(四)气体的相对分子质量的计算方法气体的相对分子质量就等于气体气体的相对分子质量就等于气体的摩尔质量的数值。的摩尔质量的数值。混合气体的相对分子质量就等于混合气体的相对分子质量就等于混合气体的平均摩尔质量的数值。混合气体的平均摩尔质量的数值。【注意】混合气体的所有组分气体均处在同【注意】混合气体的所有组分气体均处在同温同压下。温同压下。【情景导入】同种水果的大小和质量均相同,同种水果【情景导入】同种水果的大小和质量均相同,同种水果每箱的质量均相同,现有每箱的质量均相同,现有33箱红富士苹果箱红富士苹果[[10000g/10000g/箱]箱],,22箱香水梨箱香水梨[[7000g/7000g/箱]箱],,55箱脆桃箱脆桃[[8000g/8000g/箱]箱],则平均,则平均11箱水果有多少克?箱水果有多少克?平均平均11箱水果的质量=箱水果的质量=所有水果总质量所有水果总质量所有水果总箱数所有水果总箱数==33箱箱×10000g/×10000g/箱+箱+22箱箱×7000g/×7000g/箱+箱+55箱箱×8000g/×8000g/箱箱1010箱箱==8400g/8400g/箱箱【问题】计算【问题】计算2.5molO2.5molO22、、2.2molN2.2molN22和和3.3molH3.3molH22的混合气体的平均摩尔质量。的混合气体的平均摩尔质量。计算混合气体的平均相对分子质量的方法:计算混合气体的平均相对分子质量的方法:混混nm.1M+总总2211MnnM.2nnM+总总2211MVVMVV.3M例例22、例、例33、例、例44例例11相对1MM44、若已知同温同压下,、若已知同温同压下,混合气体对某气体(混合气体对某气体(MM11)的相对密度为)的相对密度为ρρ相对相对,,则则例例55例题例题(求混合气体平均相对分子质量)(求混合气体平均相对分子质量)1.1.由由8gO8gO22和和28gN28gN22组成的混合气体的平均相对组成的混合气体的平均相对分子质量是多少?分子质量是多少?2.2.相同条件下,氮气和氧气以相同条件下,氮气和氧气以1:31:3体积比混合,体积比混合,求混合气体的平均相对分子质量。求混合气体的平均相对分子质量。3.3.已知二氧化碳和氧气的混合气体其平均相对已知二氧化碳和氧气的混合气体其平均相对分子质量为分子质量为3636,求二氧化碳和氧气的体积,求二氧化碳和氧气的体积比。比。28.828.831311:21:2例题例题(求混合气体平均相对分子质量)(求混...