化学平衡状态,就是在一定条件下可逆反应里,当正反应速率与逆反应速率相等时,反应混合物中各组成成分的百分含量保持不变的状态
1、定义:强调四点条件:一定条件(温度、浓度与压强)本质:正反应速率=逆反应速率现象:各组分百分含量(或质量)、浓度(或体积分数)等保持不变对象:可逆反应(一)化学平衡状态的概念与特征正反应速率逆反应速率相等时间速率“特征量一定,达到平衡”2、化学平衡状态的特征(2)动:动态平衡(正逆反应仍在进行)(3)等:正反应速率=逆反应速率≠0(4)定:反应混合物中各组分的浓度保持不变,各组分的百分含量一定
(5)变:条件变化,化学平衡状态将被破坏,直到在新的条件下建立新的平衡
(1)逆:研究对象可逆反应
同:条件相同,某一可逆反应无论是从正反应开始还是从逆反同:条件相同,某一可逆反应无论是从正反应开始还是从逆反应开始,最终均可达到同一平衡状态
应开始,最终均可达到同一平衡状态
(对同一物质而言)(各种物质)(等效平衡)1
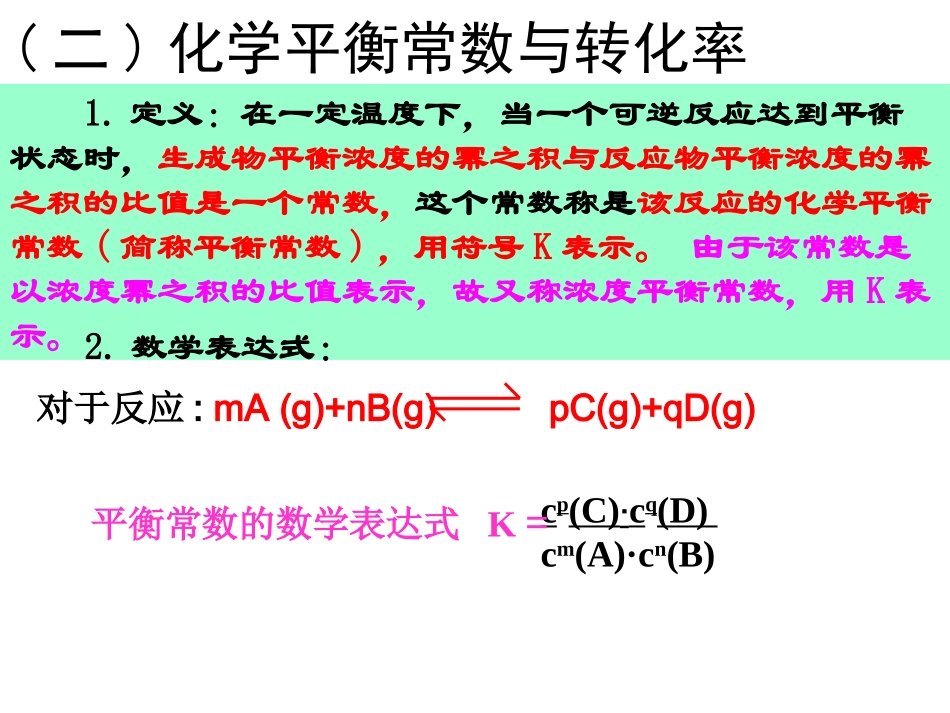
定义:在一定温度下,当一个可逆反应达到平衡状态时,生成物平衡浓度的幂之积与反应物平衡浓度的幂之积的比值是一个常数,这个常数称是该反应的化学平衡常数(简称平衡常数),用符号K表示
由于该常数是以浓度幂之积的比值表示,故又称浓度平衡常数,用K表示
(二)化学平衡常数与转化率对于反应:mA(g)+nB(g)pC(g)+qD(g)cp(C)·cq(D)cm(A)·cn(B)平衡常数的数学表达式K=2
数学表达式:1)如果反应中有固体和纯液体参加,它们的浓度不应写在平衡关系式中,因为它们的浓度是固定不变的,化学平衡关系式中只包括气态物质和溶液中各溶质的浓度
如:CaCO3(s)CaO(s)+CO2(g)CO2(g)+H2(g)CO(g)+H2O(l)注意:书写平衡常数关系式的规则K=c(CO2)K=c(CO)/[c(CO2)·c(H2)]再如:稀溶液中进