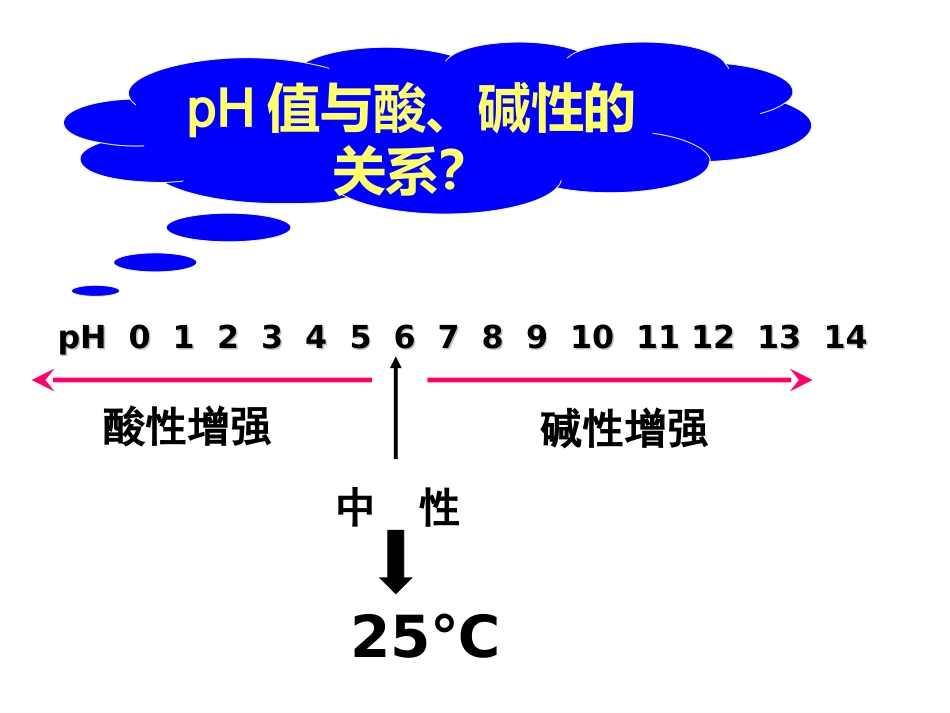
pH值与酸、碱性的关系
pH01234567891011121314pH01234567891011121314酸性增强中性碱性增强25℃溶液的酸碱性---正误判断1、如果[H+]不等于[OH-]则溶液一定呈现酸碱性
2、在水中加酸会抑制水的电离,电离程度减小
3、如果[H+]/[OH-]的值越大则酸性越强
4、任何水溶液中都有[H+]和[OH-]
5、[H+]等于10-6mol/L的溶液一定呈现酸性
6、对水升高温度电离程度增大,酸性增强
1、如果[H+]不等于[OH-]则溶液一定呈现酸或碱性
2、在水中加酸会抑制水的电离,电离程度减小
3、如果[H+]/[OH-]的值越大则酸性越强
4、任何水溶液中都有[H+]和[OH-]
5、[H+]等于10-6mol/L的溶液一定呈现酸性
6、对纯水升高温度电离程度增大,酸性增强
有关溶液中有关溶液中pHpH的计算的计算例1、标准状况下,将1
12LHCl气体溶于1L水中,加水稀释至5L,求所得溶液的pH
05mol/L的H2SO4溶液中,c(H+)=
,C(OH-)=
;由水电离出来的c(H+)=
01mol/L的NaOH溶液的pH为多少
◆强酸、强碱溶液中pH的求算:例5、将pH=12的NaOH溶液稀释100倍,求稀释后溶液的pH
例例44、将、将pH=3pH=3的的HClHCl溶液稀释溶液稀释100100倍,求稀释后溶液的倍,求稀释后溶液的pHpH
◆强酸、强碱溶液稀释后溶液pH的求算:思考:将将pH=6pH=6的的HClHCl溶液稀释溶液稀释10001000倍,求稀释后溶液的倍,求稀释后溶液的pHpH
例例66、将、将99mL0
1mol/L99mL0
1mol/L的的HClHCl与与101m101mL0
1mol/LL0
1mol/L的的NaOHNaOH溶液混合,溶液混合,体积变体积变