〔Ⅱ〕实验部分实验一蛋白质含量测定法本实验的目的是学会各种蛋白质含量的测定方法
了解各种测定方法的基本原理和优缺点
蛋白质含量测定法,是生物化学研究中最常用、最基本的分析方法之一
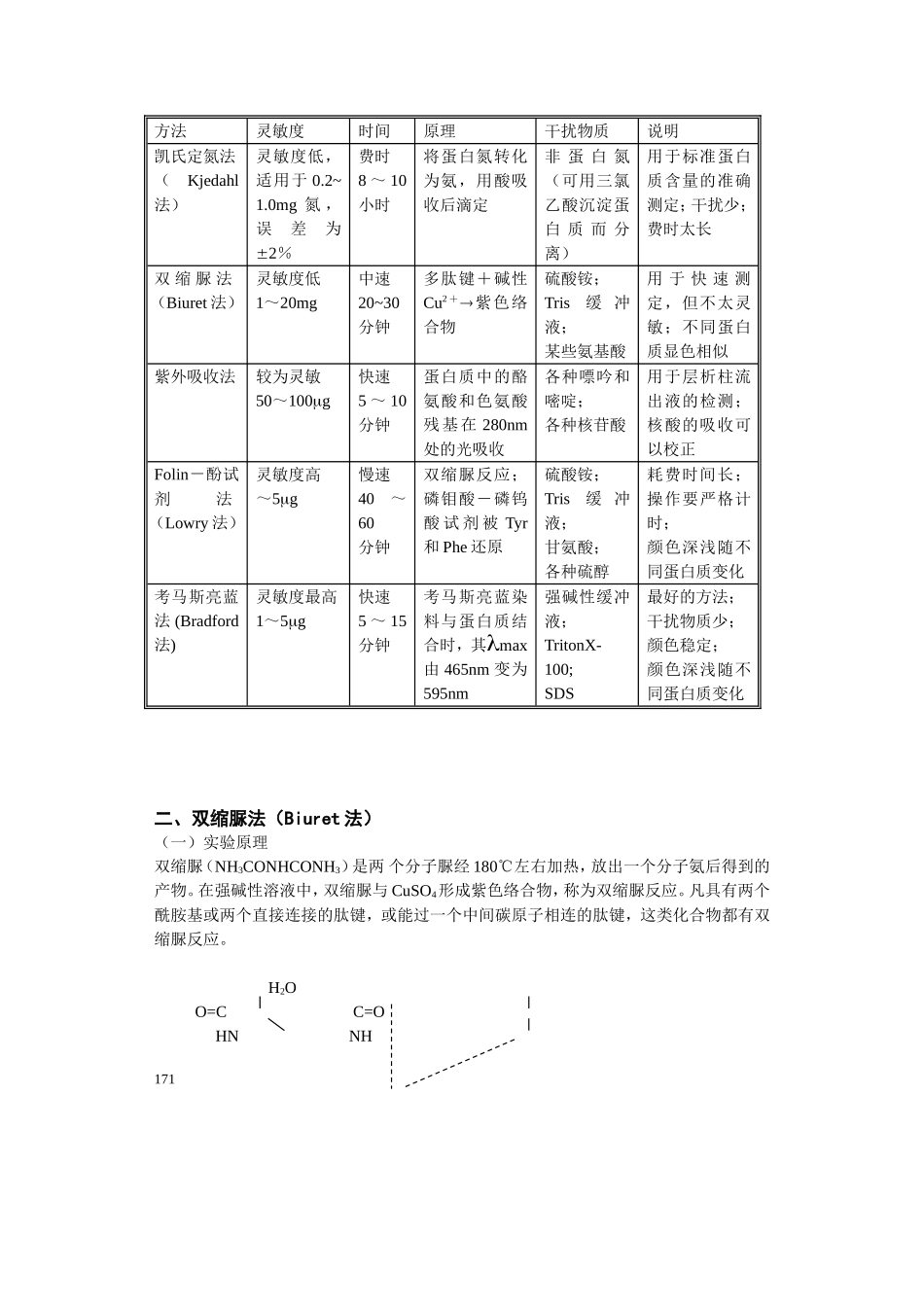
目前常用的有四种古老的经典方法,即定氮法,双缩尿法(Biuret法)、Folin-酚试剂法(Lowry法)和紫外吸收法
另外还有一种近十年才普遍使用起来的新的测定法,即考马斯亮蓝法(Bradford法)
其中Bradford法和Lowry法灵敏度最高,比紫外吸收法灵敏10~20倍,比Biuret法灵敏100倍以上
定氮法虽然比较复杂,但较准确,往往以定氮法测定的蛋白质作为其他方法的标准蛋白质
值得注意的是,这后四种方法并不能在任何条件下适用于任何形式的蛋白质,因为一种蛋白质溶液用这四种方法测定,有可能得出四种不同的结果
每种测定法都不是完美无缺的,都有其优缺点
在选择方法时应考虑:①实验对测定所要求的灵敏度和精确度;②蛋白质的性质;③溶液中存在的干扰物质;④测定所要花费的时间
考马斯亮蓝法(Bradford法),由于其突出的优点,正得到越来越广泛的应用
一、微量凯氏(Kjeldahl)定氮法样品与浓硫酸共热
含氮有机物即分解产生氨(消化),氨又与硫酸作用,变成硫酸氨
经强碱碱化使之分解放出氨,借蒸汽将氨蒸至酸液中,根据此酸液被中和的程度可计算得样品之氮含量
若以甘氨酸为例,其反应式如下:CH2COOH+3H2SO42CO2+3SO2+4H2O+NH3(1)NH22NH3+H2SO4(NH4)2SO4(2)(NH4)2SO4+2NaOH2H2O+Na2SO4+2NH3(3)反应(1)、(2)在凯氏瓶内完成,反应(3)在凯氏蒸馏装置中进行
为了加速消化,可以加入CuSO4作催化剂,K2SO4以提高溶液的沸点
收集氨可用硼酸溶液,滴定则用强酸
实验和计算方法这里从略
计算所得结果为样品总氮量,如