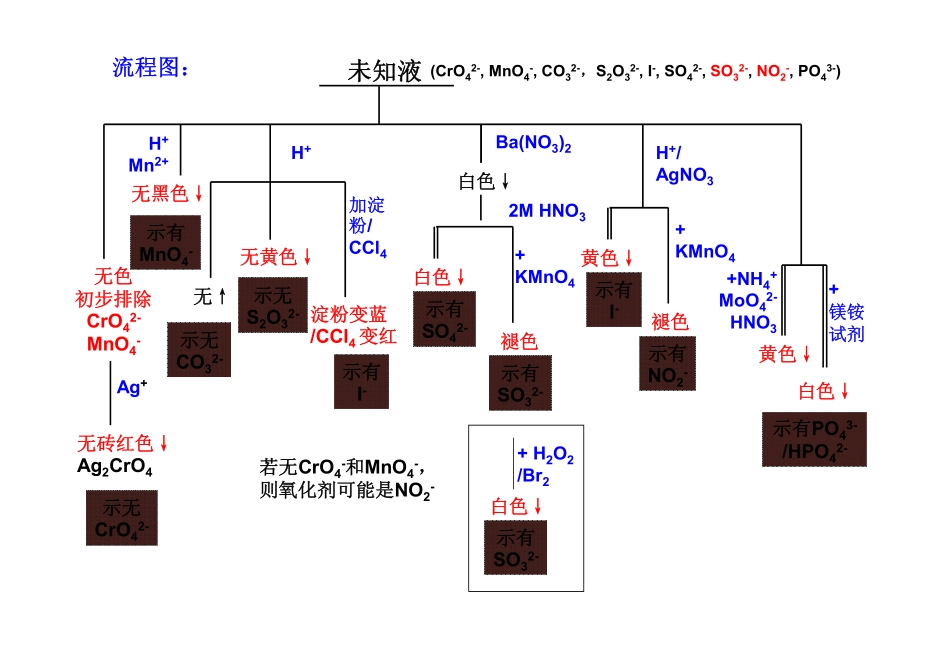
阴离子鉴别总结未知液无色初步排除CrO42-MnO4-Ag+无砖红色↓Ag2CrO4示无CrO42-H+Mn2+无黑色↓示有MnO4-H+无↑示无CO32-无黄色↓示无S2O32-加淀粉/CCl4淀粉变蓝/CCl4变红示有I-若无CrO4-和MnO4-,则氧化剂可能是NO2-Ba(NO3)2白色↓白色↓示有SO42-+KMnO4褪色示有SO32-2MHNO3H+/AgNO3示有I-+KMnO4褪色示有NO2-黄色↓+NH4+MoO42-HNO3+镁铵试剂黄色↓白色↓示有PO43-/HPO42-(CrO42-,MnO4-,CO32-,S2O32-,I-,SO42-,SO32-,NO2-,PO43-)流程图:+H2O2/Br2示有SO32-白色↓注意事项不同酸碱性条件下一些高价态氧化物的颜色会发生变化(CrO42-,MnO4-)I2在碱性条件下会发生歧化S2O32-的检验:Ag+区别与碱性条件下向体现中加入Ag+的状况对比实验,对照实验SO2与品红:酸性条件下,品红会变成橙色,随着酸性的增强颜色变淡,在碱性条件下品红试液褪色
此外在酸性条件下NO2-也能使品红褪色)体系中加入酸进行酸化时需注意:Cl-~MnO4-课后思考题如果体系中还存在Cl-,Br-,SiO3-,Ac-,AsO43-如何设计流程进行检验
本次实验内容实验40砷锑铋实验48未知物鉴别实验(五)实验48未知物鉴别实验五——阳离子的系统分析法[Cr(H2O)6]3+蓝紫色[Co(H2O)6]2+玫瑰红[Ni(H2O)6]2+淡绿色[Fe(H2O)6]2+淡绿色[Fe(H2O)6]3+淡紫色[Mn(H2O)6]2+粉红色阳离子鉴别的系统分析法颜色的干扰[CrCl(H2O)5]2+绿色[Co(NH4)6]2+褐色[Co(NCS)4]2+蓝绿色[Co(NH3)5(H2O)]3+红色[Fe(OH)(H2O)5]2