第6章第二节溶液组成的表示(第2课时)【学习目标】1
知道溶质质量分数与溶液浓稀的关系
掌握溶质质量分数的概念3
掌握溶质质量分数与溶液的稀释和浓缩的计算【学习重点】掌握溶质质量分数与溶液的稀释和浓缩的计算【学习难点】掌握与溶液溶质质量分数有关计算题的关键:找准题目中的不变量
【学习过程】一、回顾、预习与交流【旧知回顾】:硫酸铜溶液的溶质是,溶剂是
盐酸溶液的溶质是,溶剂是
铁与稀硫酸恰好完全反应后,溶质是,溶剂是
30g植物油与10g汽油形成的溶液,溶质是,溶剂是
30g酒精与10g水形成的溶液,溶质是,溶剂是
白磷溶解于二硫化碳中,叫做溶液氧化钙溶于足量的水中,叫做溶液【新知导学】:溶液组成的表示方法:阅读教材P161-162,(注:ω是希腊小写字母,读作欧米伽)二、合作、研讨与点拨活动一、根据公式完成下列问题(1)根据公式完成下表:溶质/g溶剂/g溶液/gω(溶质)蔗糖溶液(1)1090蔗糖溶液(2)1040蔗糖溶液(3)6040蔗糖溶液(4)2080(2)某食盐水的溶质质量分数为25%,它表示什么含义
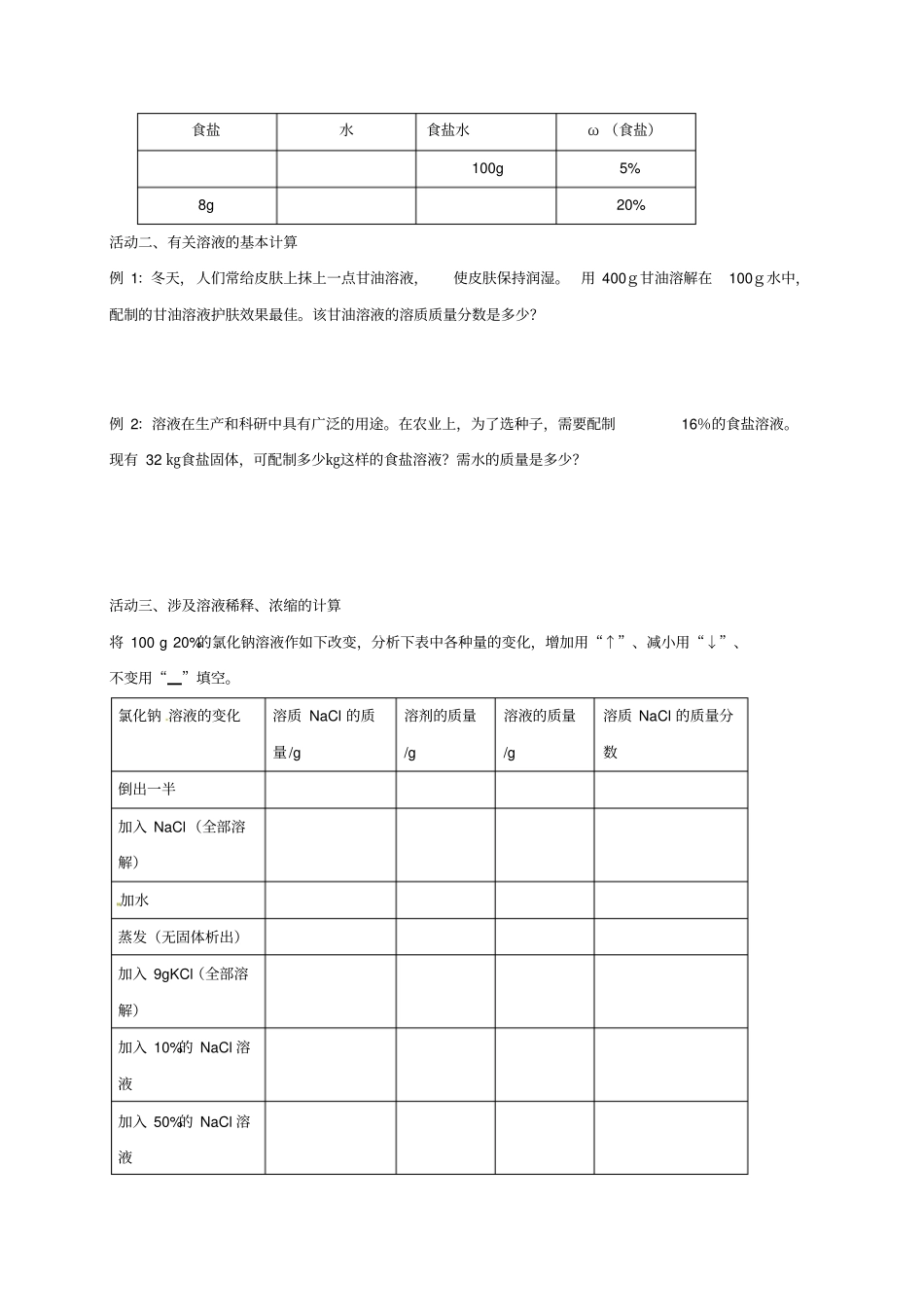
(3)变式溶液的溶质质量分数(ω溶质)=×100%食盐水食盐水ω(食盐)100g5%8g20%活动二、有关溶液的基本计算例1:冬天,人们常给皮肤上抹上一点甘油溶液,使皮肤保持润湿
用400g甘油溶解在100g水中,配制的甘油溶液护肤效果最佳
该甘油溶液的溶质质量分数是多少
例2:溶液在生产和科研中具有广泛的用途
在农业上,为了选种子,需要配制16%的食盐溶液
现有32㎏食盐固体,可配制多少㎏这样的食盐溶液
需水的质量是多少
活动三、涉及溶液稀释、浓缩的计算将100g20%的氯化钠溶液作如下改变,分析下表中各种量的变化,增加用“↑”、减小用“↓”、不变用“▁”填空
氯化钠溶液的变化溶质NaCl的质量/g溶剂的质量/g溶液的质量/g溶质NaCl的质量分数倒出一半加入N