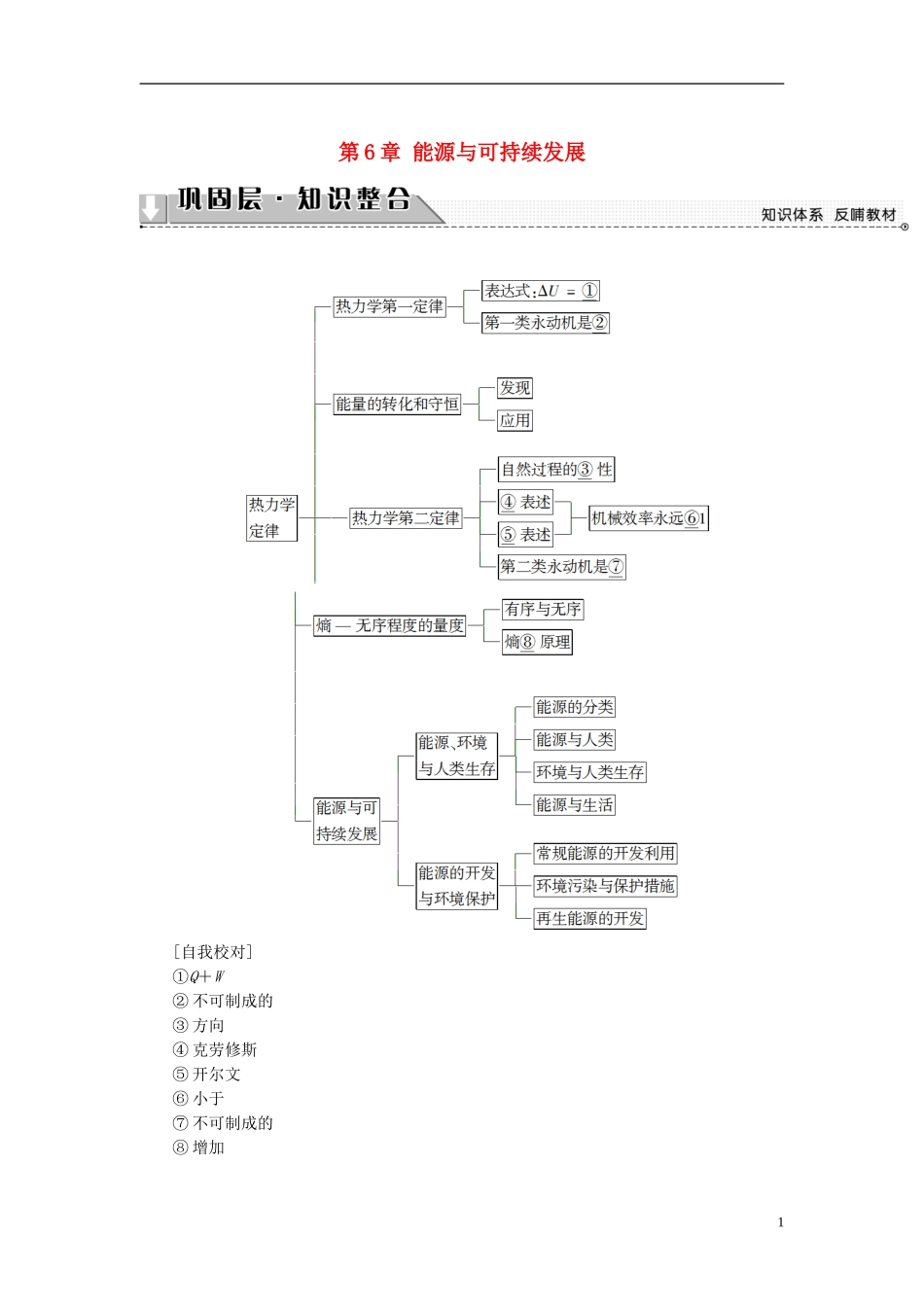
第6章能源与可持续发展[自我校对]①Q+W②不可制成的③方向④克劳修斯⑤开尔文⑥小于⑦不可制成的⑧增加1热力学第一定律与能量守恒热力学第一定律是能量守恒定律在热学中的具体表现形式.它给出了做功和热传递在改变物体内能上是等价的.热力学第一定律揭示了内能的增量(ΔU)与外界对物体做的功(W)和物体从外界吸收的热量(Q)之间的关系,即ΔU=W+Q,正确理解公式的意义及符号的含义是解决本类问题的关键.(1)外界对物体做功,W>0;物体对外界做功,W<0;(2)物体从外界吸热,Q>0;物体向外界放热,Q<0;(3)ΔU>0,物体的内能增加;ΔU<0,物体的内能减少.解题思路:分析题干,确定改变内能的方式(W、Q)→判断W、Q的符号→代入公式ΔU=W+Q→得出结论注意的问题(1)只有绝热过程时Q=0,ΔU=W,用做功可判断内能的变化.(2)只有在气体体积不变时,W=0,ΔU=Q,用吸热、放热情况可判断内能的变化.(3)若物体内能不变,即ΔU=0,W和Q不一定等于零,而是W+Q=0,功和热量符号相反,大小相等,因此判断内能变化问题一定要全面考虑.(4)对于气体,做功W的正负一般要看体积变化,气体体积缩小,W>0;气体体积增加,W<0
如图51所示的圆柱形容器内用活塞密封一定质量的气体,已知容器横截面积为S
活塞重为G,大气压强为p0
若活塞固定,密封气体温度升高1℃,需吸收的热量为Q1;若活塞不固定,且可无摩擦滑动,仍使密封气体温度升高1℃,需吸收的热量为Q2
图51问Q1和Q2哪个大些
气体在定容下的比热容与在定压下的比热容为什么会不同
【导学号:30110069】【解析】设密闭气体温度升高1°C,内能的增量为ΔU,则有ΔU=Q1①ΔU=Q2+W②因气体体积膨胀,W<0,故Q1>Q2由此可见,质量相等的同种气体,在定容和定压两种不同情况下,尽管温度变化相同,但2吸收的热量不同,所以同种