第二节离子反应离子方程式考点(一)电解质及其电离【精讲精练快冲关】[知能学通]1
电解质与非电解质电解质非电解质概念在水溶液或熔融状态下能导电的化合物在水溶液和熔融状态下均不能导电的化合物关键词“或、化合物”“和、化合物”满足条件导电不导电实质自身电离出离子自身不能电离出离子注意用“自身”能否电离可确定是否为电解质2
强电解质和弱电解质(1)强、弱电解质的比较强电解质弱电解质电离程度完全部分电离平衡不存在存在溶液中微粒种类离子、水分子离子、水分子、弱电解质分子(2)注意事项电解质的强弱与其溶解性无关
某些盐如BaSO4等虽难溶于水,但溶于水的部分是完全电离的,故它们是强电解质
相反,能溶于水的未必都是强电解质,如CH3COOH等虽然能溶于水,但溶解时只有部分电离,故它们是弱电解质
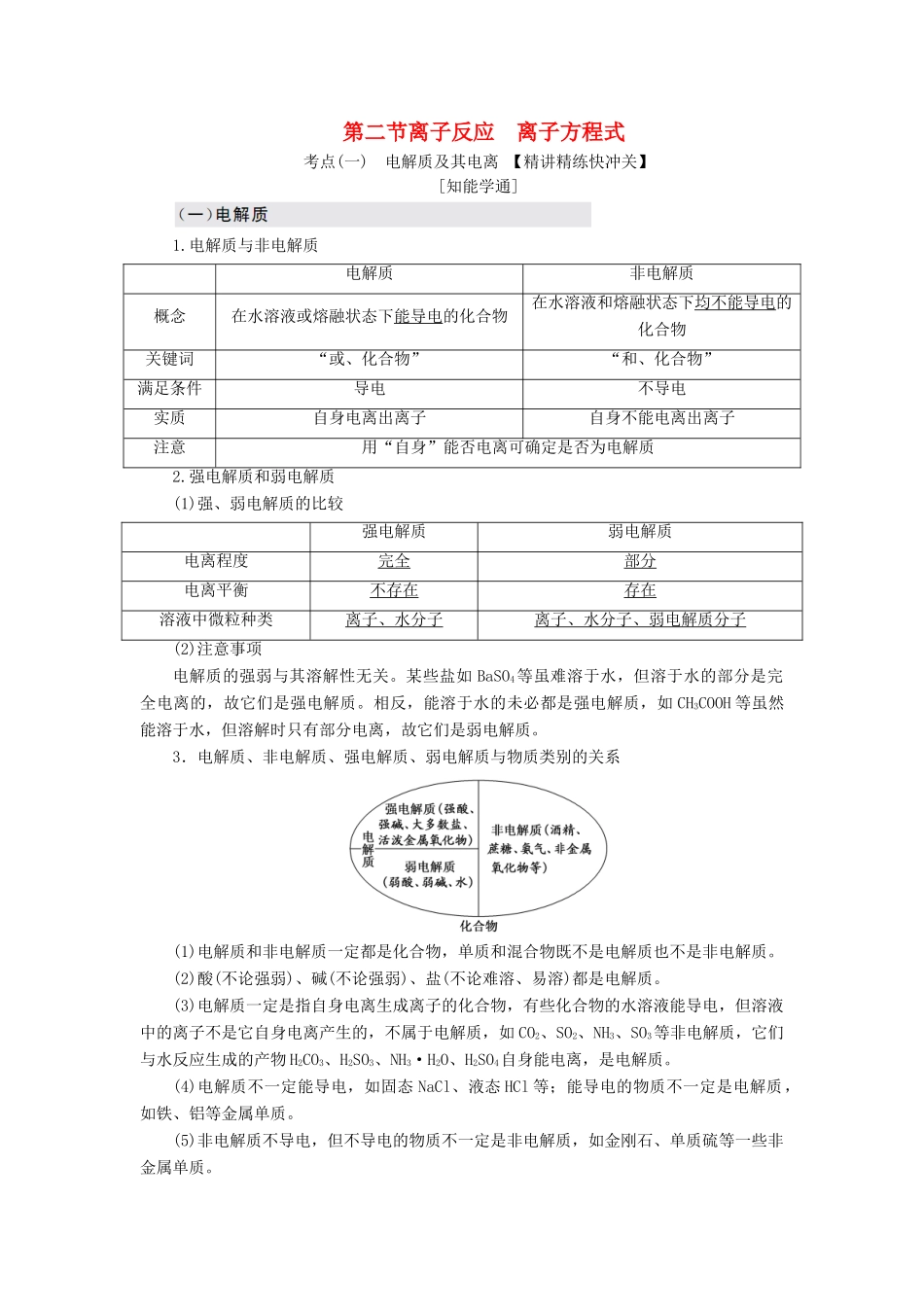
3.电解质、非电解质、强电解质、弱电解质与物质类别的关系(1)电解质和非电解质一定都是化合物,单质和混合物既不是电解质也不是非电解质
(2)酸(不论强弱)、碱(不论强弱)、盐(不论难溶、易溶)都是电解质
(3)电解质一定是指自身电离生成离子的化合物,有些化合物的水溶液能导电,但溶液中的离子不是它自身电离产生的,不属于电解质,如CO2、SO2、NH3、SO3等非电解质,它们与水反应生成的产物H2CO3、H2SO3、NH3·H2O、H2SO4自身能电离,是电解质
(4)电解质不一定能导电,如固态NaCl、液态HCl等;能导电的物质不一定是电解质,如铁、铝等金属单质
(5)非电解质不导电,但不导电的物质不一定是非电解质,如金刚石、单质硫等一些非金属单质
(6)溶液导电性的强弱只与溶液中离子浓度及离子所带电荷数有关,与电解质的强弱无直接关系
电离电解质在水溶液中或熔融状态下,离解成自由移动离子的过程
2.电离方程式(1)强电解质:完全电离,用“===”连接
(2)弱电解质:部分电离,用“”连接