河南省郑州市第三十一中学九年级化学下册《溶解度》导学案【学习目标】1
通过自学及实物展示能描述金属铝的物理性质
通过实验及新旧知识结合学习掌握金属铝的还原性
初步知道合金的概念,能列举常见金属合金材料在生产生活中的重要应用
【重点难点】金属铝的还原性【学案导学】元素周期表中110多种元素,约有4/5是金属元素,其中常见的金属有哪些呢
你对这些金属的物理性质及化学性质知道多少呢
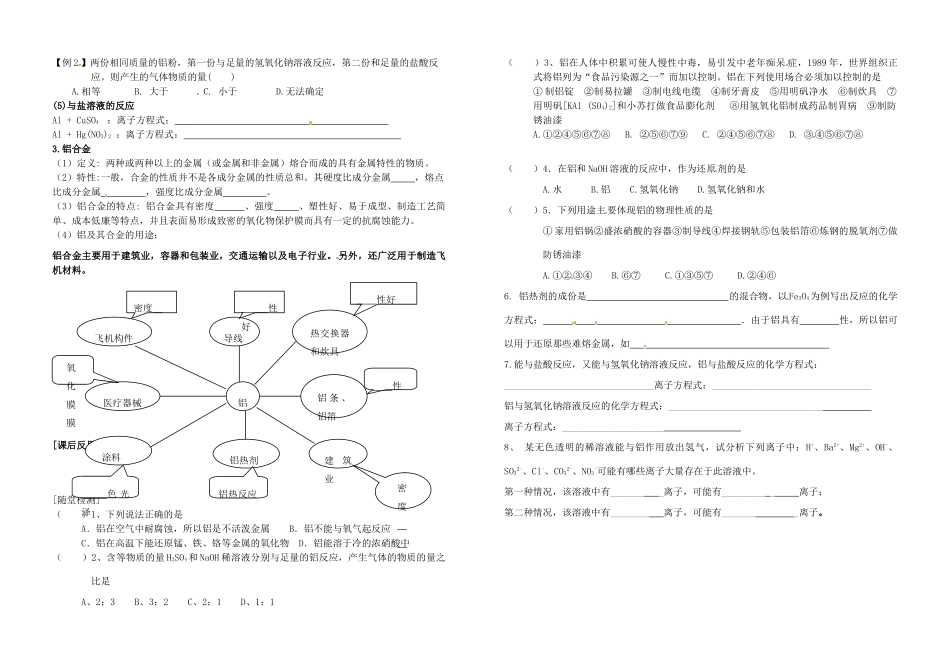
一、铝与铝合金【自主学习】阅读教材P116,结合实物了解铝的物理性质1、铝的物理性质:铝密度较,仅为钢的1/3左右;熔点较;硬度较的色金属,有光泽;具有良好的、性,导电性仅次于,且有非常好的性
2.铝的化学性质【小组讨论学习】回顾钠、镁、铁单质的性质,然后进行类推和假设,从铝属类别的角度预测铝可能的化学性质
金属单质的反应规律:①与其它非金属单质反应
如②与水的反应
如③与酸的反应
如④某些盐的反应
如⑤与某些氧化物的反应
如(1)与非金属反应演示实验1:铝箔的燃烧(课本116页观察与思考)现象:铝箔在氧气中剧烈燃烧,发出耀眼的,生成固体
方程式:应用:制燃烧弹,信号弹,火箭推进剂思考:①集气瓶的底部要放一些水(或细沙),其作用是什么
②完成下列方程式Al+Cl2===Al+S===(2)与某些氧化物反应演示实验2:铝热反应(课本116页观察与思考)现象:,,方程式:思考:①从四大基本反应类型来看,上述反应应属于哪一类
哪些金属氧化物可以与铝粉发生类似的反应
结论:Al将活泼性比其的金属从其氧化物中置换出来,放出大量的热,新生成的金属呈态且与Al2O3容易分离
②怎样证明反应放出大量的热
③镁条、氯酸钾的作用是什么
【归纳总结】铝热反应:Al与金属氧化物在较高的温度下,发生置换反应,并放出大量的热
铝热剂:铝粉和金属氧化物(活泼性比其的金属氧化物)的称为铝热剂
铝热反应:Al+M