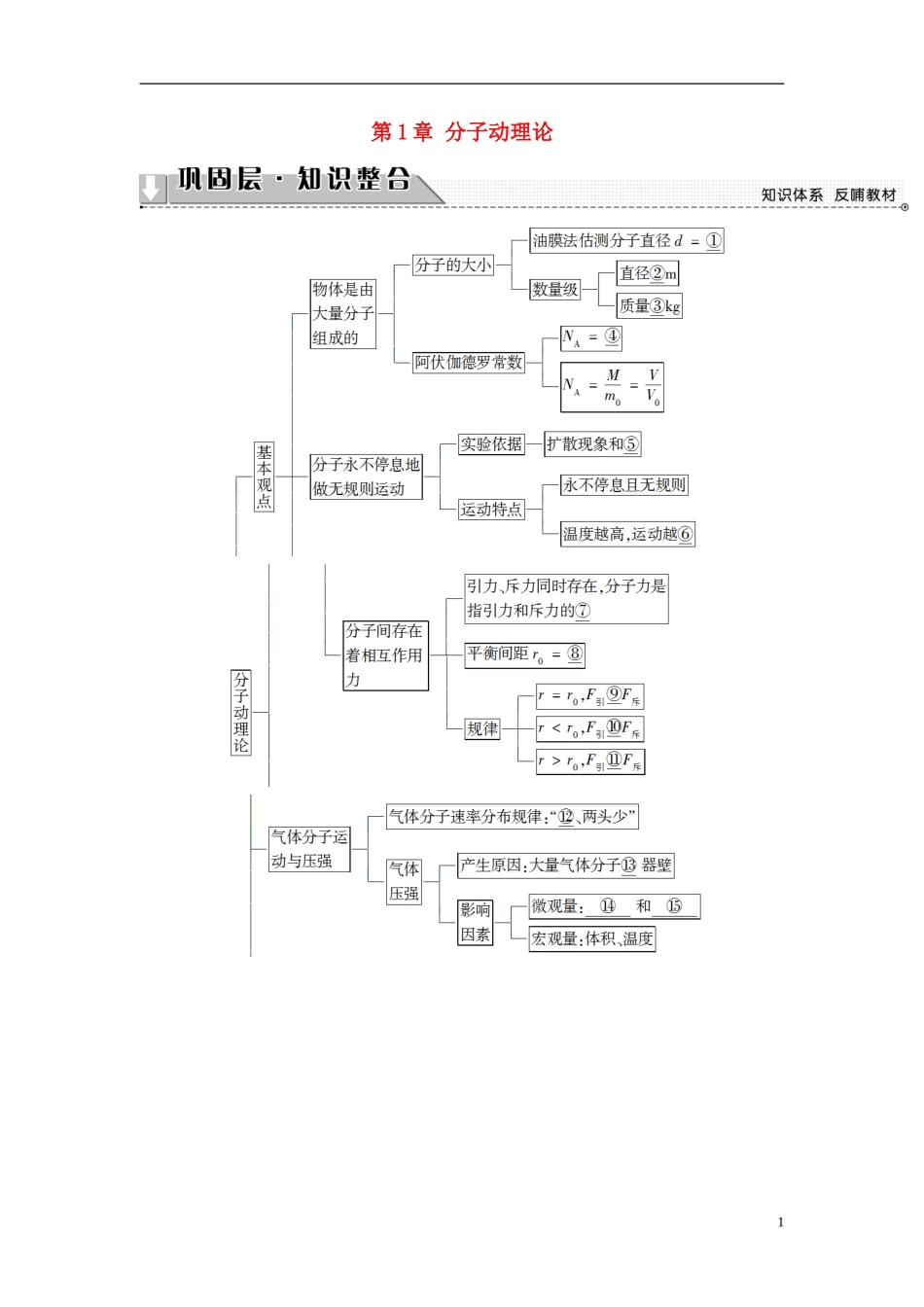
第1章分子动理论1[自我校对]①②10-10③10-27~10-25④6
02×1023mol-1⑤布朗运动⑥剧烈⑦合力⑧10-10m⑨=⑩⑫中间多⑬频繁撞击⑭分子数密度⑮分子平均动能⑯平均动能⑰物体的质量⑱温度⑲体积⑳热传递分子微观量的估算21
对微观量的估算,首先要建立微观模型,对于固体和液体,可以把它们看成是分子一个挨一个紧密排列的.计算时将物质的摩尔体积分成NA等份,每一等份就是一个分子.在估算分子直径时,设想分子是一个紧挨着一个的小球;在估算分子间距离时,设想每一个分子是一个立方体,立方体的边长即为分子间的距离.2.气体分子不是紧密排列的,所以上述模型对气体不适用,但上述模型可以用来估算气体分子间的平均距离.3.阿伏伽德罗常数是联系微观物理量与宏观物理量的桥梁,它把摩尔质量、摩尔体积这些宏观物理量与分子质量、分子大小等微观物理量联系起来.有关计算主要有:(1)已知物质的摩尔质量M,借助于阿伏伽德罗常数NA,可以求得这种物质的分子质量m0=
(2)已知物质的摩尔体积VA,借助于阿伏伽德罗常数NA,可以计算出这种物质的一个分子所占据的体积V0=
(3)若物体是固体或液体,可把分子视为紧密排列的球形分子,可估算出分子直径d=
(4)依据求得的一个分子占据的体积V0,可估算分子间距,此时把每个分子占据的空间看做一个小立方体模型,所以分子间距d=,这对气体、固体、液体均适用.(5)已知物体的体积V和摩尔体积VA,求物体的分子数N,则N=
(6)已知物体的质量m和摩尔质量M,求物体的分子数N,则N=NA
用长度放大600倍的显微镜观察布朗运动.估计放大后的小颗粒(碳)体积为0
1×10-9m3,碳的密度是2
25×103kg/m3,摩尔质量是1
2×10-2kg/mol,阿伏伽德罗常数为6
02×1023mol-1,则该小碳粒含分子数约为多少个
(取一位有效数字)【解析】已知