第5课时化学能与电能(3)——电解原理及应用(过基础)知识点一电解原理1.电解池(1)电解池:把电能转化为化学能的装置
(2)构成条件①有与直流电源相连的两个电极;②电解质溶液(或熔融盐);③形成闭合回路
(3)工作原理(以惰性电极电解CuCl2溶液为例)总反应离子方程式:Cu2++2Cl-=====Cu+Cl2↑①电极阴极:与电源负极相连,得到电子,发生还原反应
阳极:与电源正极相连,失去电子,发生氧化反应
②电子和离子的移动方向(惰性电极)[提醒]①金属活动性顺序中银以前的金属(含银)作电极时,由于金属本身可以参与阳极反应,称为金属电极或活性电极(如Zn、Fe、Cu、Ag等);金属活动性顺序中银以后的金属或非金属作电极时,称为惰性电极,主要有铂(Pt)、石墨等
②电解时,在外电路中有电子通过,而在溶液中是靠离子移动导电,即电子不通过电解质溶液
2.电极反应式的书写步骤[提醒]①书写电解池的电极反应式时,可以用实际放电的离子表示,但书写电解池的总反应时,弱电解质要写成分子式
如用惰性电极电解食盐水时,阴极反应式为2H++2e-===H2↑(或2H2O+2e-===H2↑+2OH-);总反应离子方程式为2Cl-+2H2O=====2OH-+H2↑+Cl2↑
②电解水溶液时,应注意放电顺序,位于H+、OH-之后的离子一般不参与放电
③Fe3+在阴极上放电时生成Fe2+而不是得到单质Fe
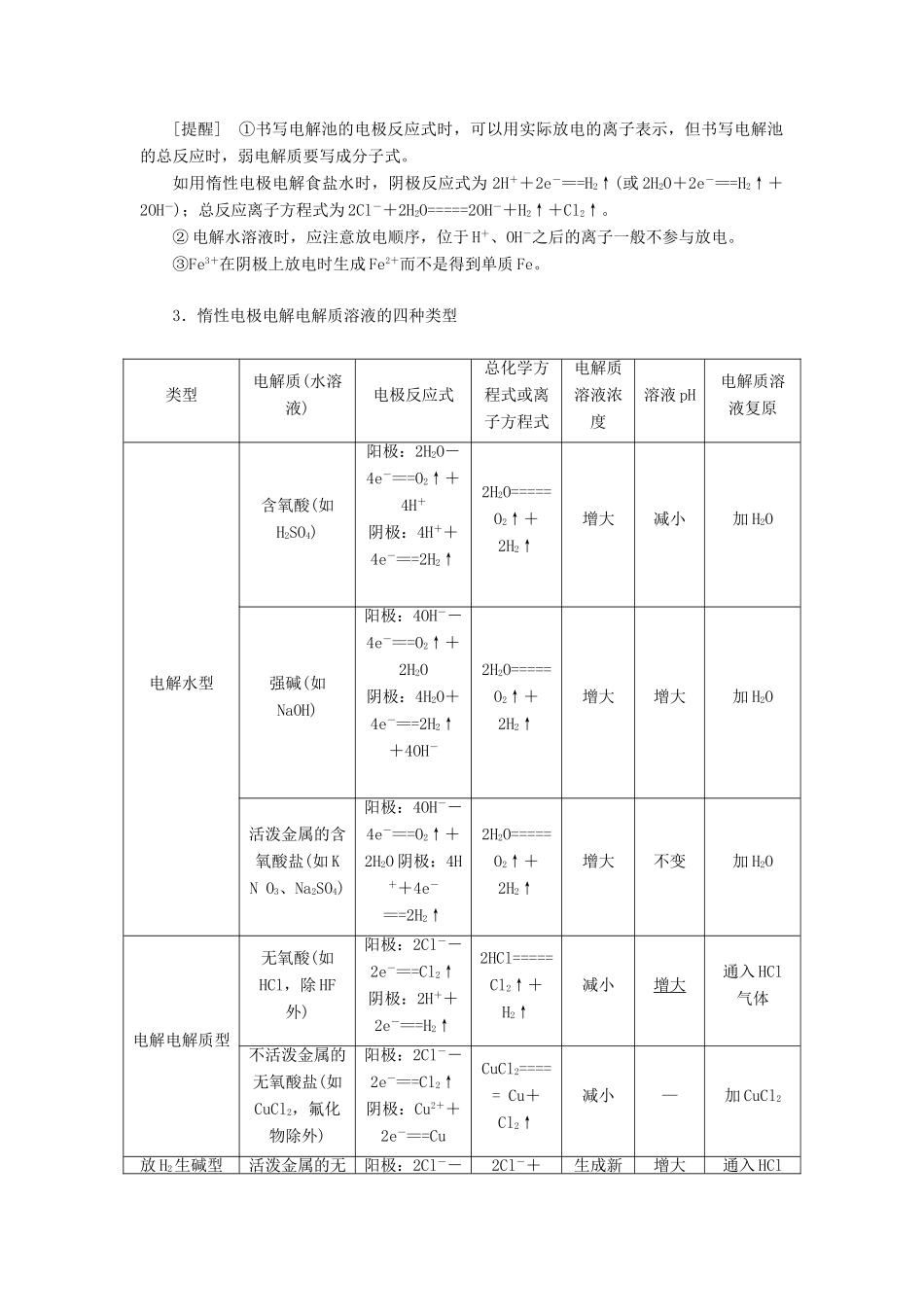
3.惰性电极电解电解质溶液的四种类型类型电解质(水溶液)电极反应式总化学方程式或离子方程式电解质溶液浓度溶液pH电解质溶液复原电解水型含氧酸(如H2SO4)阳极:2H2O-4e-===O2↑+4H+阴极:4H++4e-===2H2↑2H2O=====O2↑+2H2↑增大减小加H2O强碱(如NaOH)阳极:4OH--4e-===O2↑+2H2O阴极:4H2O+4e-===2H2↑+4OH-2H2