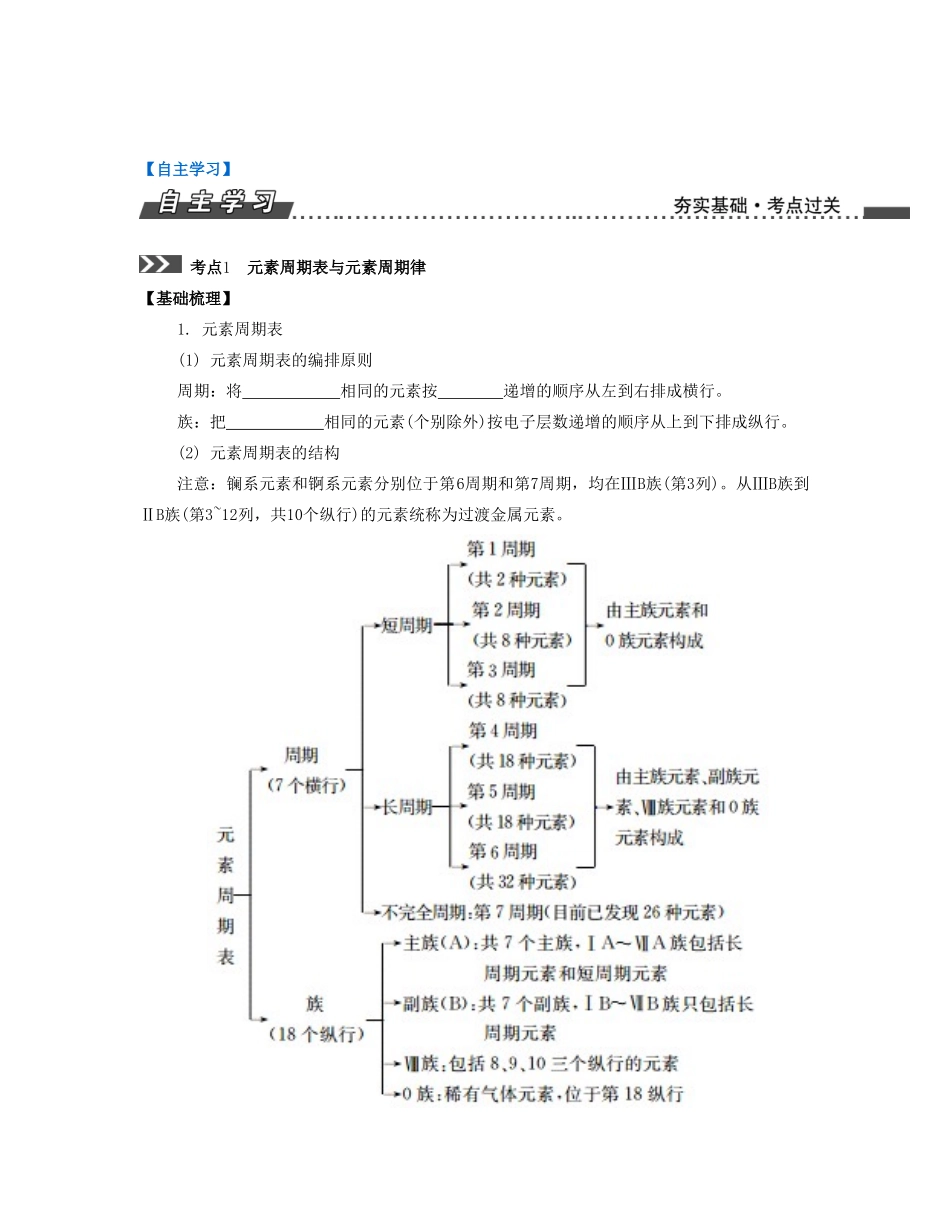
课时5元素周期表化学键(本课时对应学生用书第22~27页)【课时导航】复习目标1.了解物质的组成、结构和性质的关系。2.了解元素周期表的结构及其应用。3.以第3周期、ⅠA和ⅦA族为例,掌握同一周期、同一主族内元素性质的递变规律与原子结构的关系。4.了解金属、非金属在元素周期表中的位置及其性质递变的规律。5.认识化学键的含义;了解离子键和共价键的形成;了解常见离子化合物和共价化合物的形成过程。6.能识别典型的离子化合物和共价化合物;能从化学键变化的角度认识化学反应的实质。知识网络问题思考问题1如何用原子结构理论来解释同一周期元素(稀有气体除外)、同一主族元素性质的变化规律?问题2离子化合物中是不是一定含有金属元素?含有共价键的化合物是不是一定是共价化合物?【自主学习】考点1元素周期表与元素周期律【基础梳理】1.元素周期表(1)元素周期表的编排原则周期:将相同的元素按递增的顺序从左到右排成横行。族:把相同的元素(个别除外)按电子层数递增的顺序从上到下排成纵行。(2)元素周期表的结构注意:镧系元素和锕系元素分别位于第6周期和第7周期,均在ⅢB族(第3列)。从ⅢB族到ⅡB族(第3~12列,共10个纵行)的元素统称为过渡金属元素。(3)元素周期表与原子结构的关系周期序数=主族序数=2.元素周期律(1)元素周期律(2)同周期、同主族元素性质的递变规律内容同周期(从左到右)同主族(自上而下)原子结构核电荷数逐渐逐渐电子层数依次逐渐原子半径逐渐逐渐元素性质主要化合价最高正价+1→+7;最低负价-4→-1最高正价=主族序数(O、F除外)金属性逐渐逐渐非金属性逐渐逐渐化合物性质最高价氧化物对应水化物酸性;碱性酸性;碱性氢化物稳定性【举题说法】例题1(2015·江苏高考)短周期主族元素X、Y、Z、W原子序数依次增大,X原子最外层有6个电子,Y是至今发现的非金属性最强的元素,Z在周期表中处于周期序数等于族序数的位置,W的单质广泛用作半导体材料。下列叙述正确的是()A.原子最外层电子数由多到少的顺序:Y、X、W、ZB.原子半径由大到小的顺序:W、Z、Y、XC.元素非金属性由强到弱的顺序:Z、W、XD.简单气态氢化物的稳定性由强到弱的顺序:X、Y、W【答案】A【解析】根据元素的描述可知X、Y、Z、W分别为O、F、Al、Si。最外层电子数由多到少的顺序为F、O、Si、Al,A正确;原子半径由大到小的顺序为Al、Si、O、F,B错误;元素非金属性由强到弱的顺序为O、Si、Al,C错误;简单气态氢化物的稳定性顺序与非金属性顺序一致,正确的顺序是F、O、Si,D错误。【题组训练】1.(2016·苏北四市一模)短周期元素X、Y、Z、W的原子序数依次增大,X在元素周期表中原子半径最小,Y原子在周期表中处于族序数等于周期序数3倍的位置,Z是最外层电子数最少的金属元素,W与Y属于同一主族。下列叙述正确的是()A.原子半径:W>Z>YB.元素W最高价氧化物对应水化物为强酸C.化合物X2Y、Z2Y中化学键的类型相同D.元素Y的简单气态氢化物的热稳定性比W的弱【答案】B【解析】X在元素周期表中原子半径最小,X是氢元素,Y原子在周期表中处于族序数等于周期序数3倍的位置,Y是氧元素,Z是最外层电子数最少的金属,原子序数大于8,是钠元素,元素W与Y属于同一主族,W是硫元素。原子半径:Na>S>O,A错误;硫酸是强酸,B正确;水中只含有共价键,氧化钠中只含有离子键,C错误;水的稳定性强于硫化氢,D错误。2.(2016·苏州一模)短周期主族元素X、Y、Z、W原子序数依次增大,X元素的单质可在自然界中形成最硬的矿石,Y原子最外层有6个电子,Z元素的氧化物可作耐高温材料且其最高价氧化物对应水化物是难溶于水的碱性物质,W与X同主族。下列叙述正确的是()A.原子最外层电子数由少到多的顺序:X=WX>Y>ZC.元素非金属性由强到弱的顺序:X、Y、WD.元素的简单气态氢化物的稳定性由强到弱的顺序:Y、X、W【答案】D【解析】自然界中最硬的矿石是金刚石,X是碳元素,Y最外层有6个电子,可能是O或S,Z元素的氧化物可作耐高温材料且其最高价氧化物对应水化物是难溶于水的碱性物质,Z是镁,则Y是O元素,W与X同主族,W是硅。氧原子最外层电子数最多,A错误;镁原子的半径最大,B错误;非金属性:O>C...