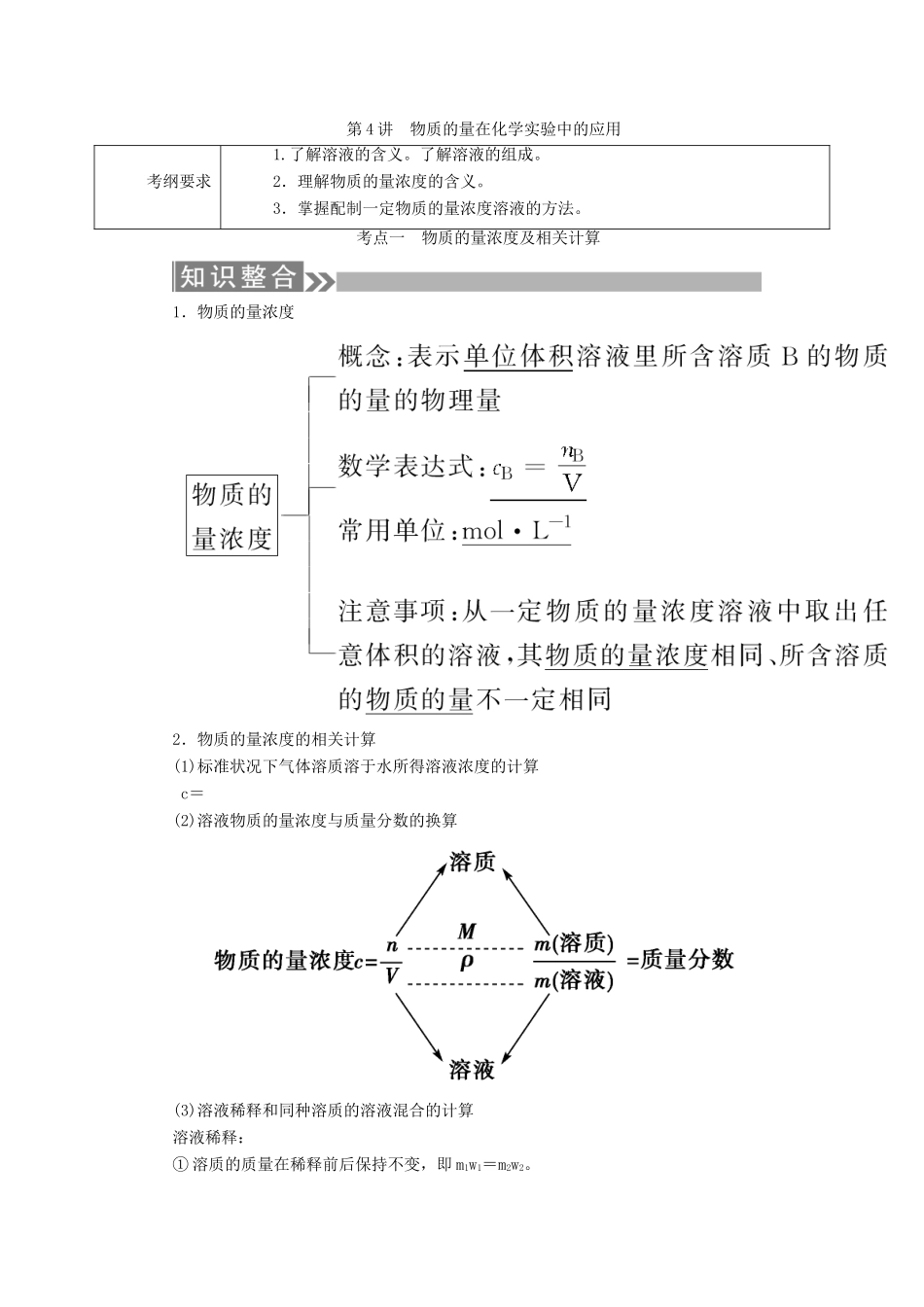
第4讲物质的量在化学实验中的应用考纲要求1
了解溶液的含义
了解溶液的组成
2.理解物质的量浓度的含义
3.掌握配制一定物质的量浓度溶液的方法
考点一物质的量浓度及相关计算1.物质的量浓度2.物质的量浓度的相关计算(1)标准状况下气体溶质溶于水所得溶液浓度的计算c=(2)溶液物质的量浓度与质量分数的换算(3)溶液稀释和同种溶质的溶液混合的计算溶液稀释:①溶质的质量在稀释前后保持不变,即m1w1=m2w2
②溶质的物质的量在稀释前后保持不变,即c1V1=c2V2
溶液混合:混合前后溶质的物质的量保持不变,即:c1V1+c2V2=c混V混
【多维思考】1.质量分数与物质的量浓度有何相同之处
提示:都可以表达出一定量溶液(1L或100g)中溶质的多少(n或m)
2.80%的H2SO4溶液与60%的H2SO4等体积混合后浓度等于70%吗
提示:不等于70%而是大于70%
有关物质的量浓度的计算(1)溶质的质量、溶液的体积和物质的量浓度之间的计算运用公式:n=,c=或运用“倍数关系”算出1L溶液中所含溶质的物质的量
(2)已知气体溶质的体积(标准状况)、水的体积和溶液的密度,计算溶液的物质的量浓度先运用n=求出溶质的物质的量,再运用V=求出溶液的体积,最后根据c=计算
(3)溶液中溶质的质量分数与物质的量浓度间的换算c=(c为溶质的物质的量浓度mol·L-1,ρ为溶液密度g·cm-3,w为溶质的质量分数,M为溶质的摩尔质量),此公式按溶液体积为1L进行推导
(4)溶液稀释和同种溶质的溶液混合的计算①原理:根据稀释或混合前后,溶液中溶质的物质的量总量不变的公式c1·V1=c2·V2、c1·V1+c2·V2=c混·V混,计算有关的量
②体积问题:体积一般不可以相加,而应运用V混=算出最后溶液的总体积
只有稀溶液稀释(或相互混合)且题中未给出稀释(或混合)后溶液的密度时,才可以忽