课题2第二课时]在一定条件下,不同的物质,其溶解能力也不相同,例如食盐比面粉在水中的溶解能力大;但是食盐和硝酸钾相比,谁的溶解能力大
怎样进行比较
在怎样的条件下,可以更好地比较不同物质溶解能力的大小
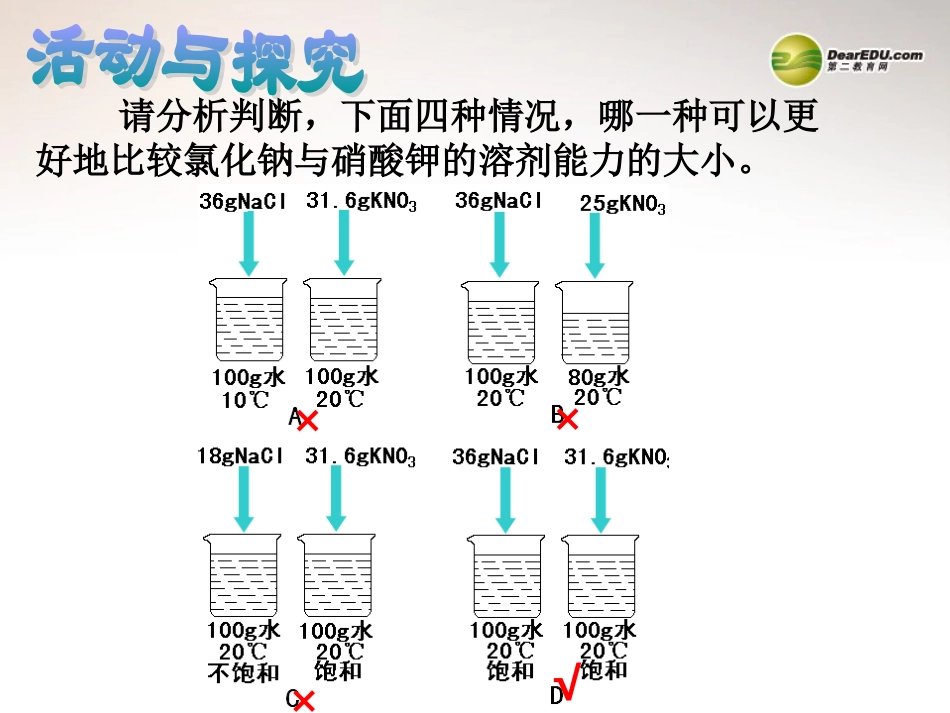
请分析判断,下面四种情况,哪一种可以更好地比较氯化钠与硝酸钾的溶剂能力的大小
×××√四要素:条件:在一定温度下标准:在100克溶剂中状态:达到饱和状态单位:克二、溶解度1、固体物质的溶解度:在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量
2、影响固体溶解度的因素:溶剂的种类溶质的种类温度√溶解度与溶质,溶剂的质量无关注意溶解性与固体溶解度的关系溶解性易溶可溶微溶难溶20ºC时的溶解度>10g1-10g0
01-1gB物质的溶解度
在____时A物质的溶解度小于B物质的溶解度
巩固练习(1)M点的含义是___________,(2)当温度为t1ºC,三种物质溶解度由小到大依次为______,当为t3ºC时,溶解度最大的是________
2、如图是A、B、C三种物质在水中的溶解度曲线,请回答:巩固练习3、图中所示是A、B两种固体物质的溶解度曲线,下列说法正确的是A
B的溶解度小于A的溶解度B
在t℃时,A的质量分数大于B的质量分数C
当A中含有少量B时,可用结晶法提纯AD
0℃时,A是微溶物质,B是易溶物质巩固练习再见