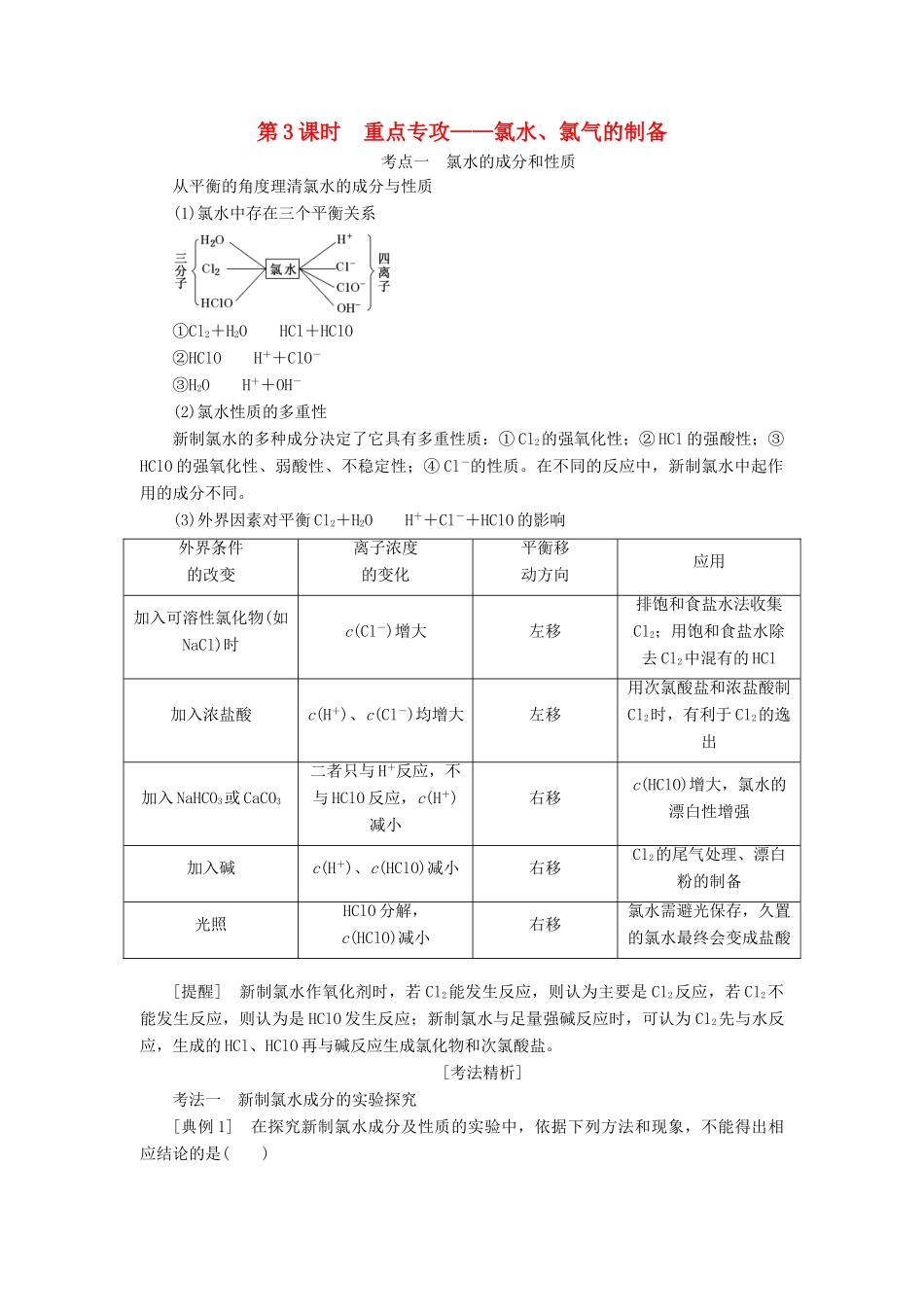
第3课时重点专攻——氯水、氯气的制备考点一氯水的成分和性质从平衡的角度理清氯水的成分与性质(1)氯水中存在三个平衡关系①Cl2+H2OHCl+HClO②HClOH++ClO-③H2OH++OH-(2)氯水性质的多重性新制氯水的多种成分决定了它具有多重性质:①Cl2的强氧化性;②HCl的强酸性;③HClO的强氧化性、弱酸性、不稳定性;④Cl-的性质
在不同的反应中,新制氯水中起作用的成分不同
(3)外界因素对平衡Cl2+H2OH++Cl-+HClO的影响外界条件的改变离子浓度的变化平衡移动方向应用加入可溶性氯化物(如NaCl)时c(Cl-)增大左移排饱和食盐水法收集Cl2;用饱和食盐水除去Cl2中混有的HCl加入浓盐酸c(H+)、c(Cl-)均增大左移用次氯酸盐和浓盐酸制Cl2时,有利于Cl2的逸出加入NaHCO3或CaCO3二者只与H+反应,不与HClO反应,c(H+)减小右移c(HClO)增大,氯水的漂白性增强加入碱c(H+)、c(HClO)减小右移Cl2的尾气处理、漂白粉的制备光照HClO分解,c(HClO)减小右移氯水需避光保存,久置的氯水最终会变成盐酸[提醒]新制氯水作氧化剂时,若Cl2能发生反应,则认为主要是Cl2反应,若Cl2不能发生反应,则认为是HClO发生反应;新制氯水与足量强碱反应时,可认为Cl2先与水反应,生成的HCl、HClO再与碱反应生成氯化物和次氯酸盐
[考法精析]考法一新制氯水成分的实验探究[典例1]在探究新制氯水成分及性质的实验中,依据下列方法和现象,不能得出相应结论的是()选项方法现象结论A观察氯水颜色氯水呈浅黄绿色氯水中含Cl2B向饱和NaHCO3溶液中加入足量氯水有无色气体产生氯水中含HClOC向红色纸条上滴加氯水红色纸条褪色氯水具有漂白性D向FeCl2溶液中滴加氯水溶液变成棕黄色氯水具有氧化性[解析]氯气为黄绿色气体,氯