乙炔的实验室制法实验室制乙炔1、学会实验室制取乙炔的原理及方法2、掌握乙炔的性质3、熟悉仪器的使用,药品的选择CaC2+2H2O→Ca(OH)2+C2H2↑圆底烧瓶、分液漏斗、小试管、导管、铁架台(带铁夹)碳化钙(CaC2)俗称电石,饱和食盐水(水)步骤实验现象实验结论及解释1.检查装置的气密性2.在圆底烧瓶里放入几小块电石
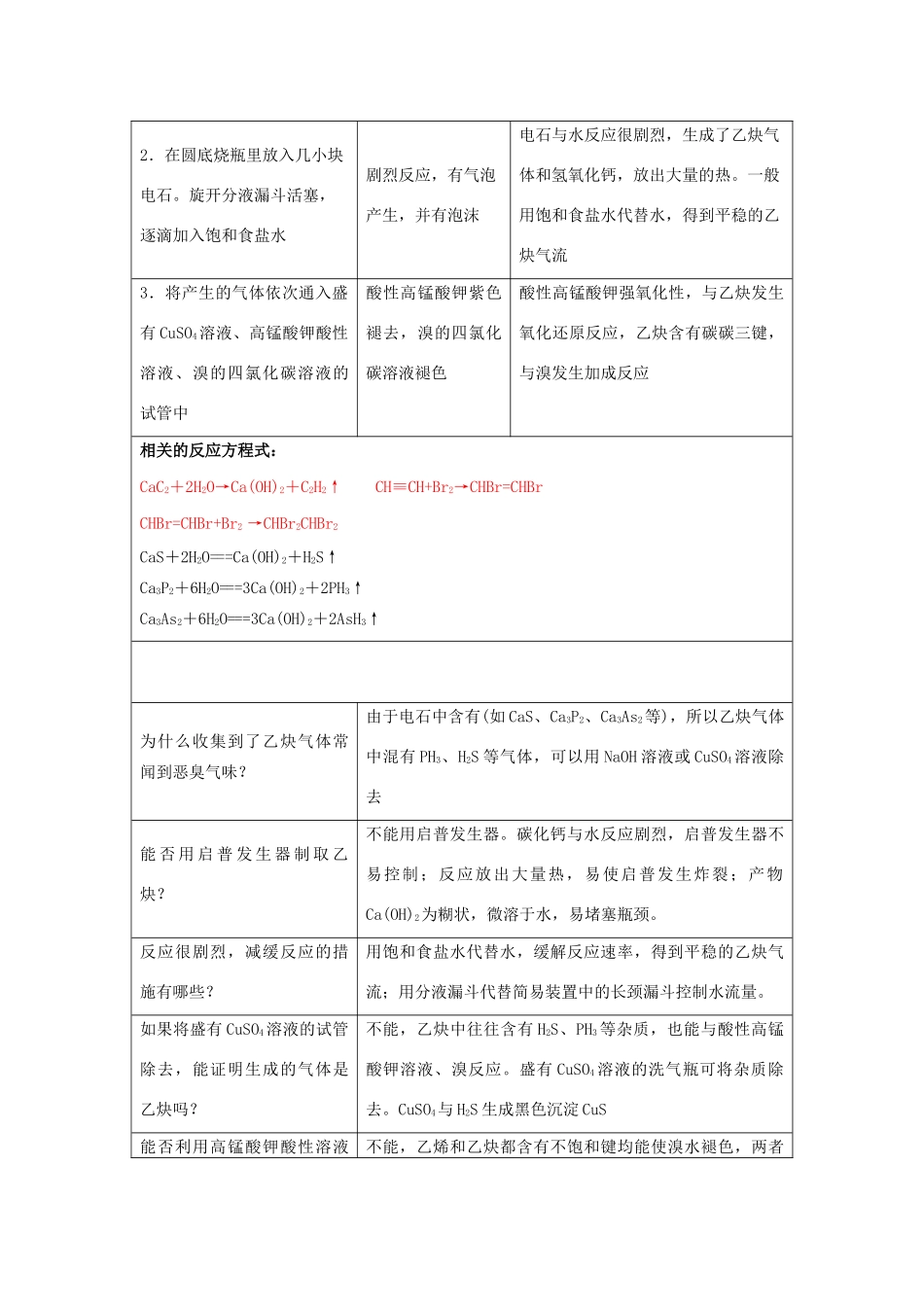
旋开分液漏斗活塞,逐滴加入饱和食盐水剧烈反应,有气泡产生,并有泡沫电石与水反应很剧烈,生成了乙炔气体和氢氧化钙,放出大量的热
一般用饱和食盐水代替水,得到平稳的乙炔气流3.将产生的气体依次通入盛有CuSO4溶液、高锰酸钾酸性溶液、溴的四氯化碳溶液的试管中酸性高锰酸钾紫色褪去,溴的四氯化碳溶液褪色酸性高锰酸钾强氧化性,与乙炔发生氧化还原反应,乙炔含有碳碳三键,与溴发生加成反应相关的反应方程式:CaC2+2H2O→Ca(OH)2+C2H2↑CH≡CH+Br2→CHBr=CHBrCHBr=CHBr+Br2→CHBr2CHBr2CaS+2H2O===Ca(OH)2+H2S↑Ca3P2+6H2O===3Ca(OH)2+2PH3↑Ca3As2+6H2O===3Ca(OH)2+2AsH3↑为什么收集到了乙炔气体常闻到恶臭气味
由于电石中含有(如CaS、Ca3P2、Ca3As2等),所以乙炔气体中混有PH3、H2S等气体,可以用NaOH溶液或CuSO4溶液除去能否用启普发生器制取乙炔
不能用启普发生器
碳化钙与水反应剧烈,启普发生器不易控制;反应放出大量热,易使启普发生炸裂;产物Ca(OH)2为糊状,微溶于水,易堵塞瓶颈
反应很剧烈,减缓反应的措施有哪些
用饱和食盐水代替水,缓解反应速率,得到平稳的乙炔气流;用分液漏斗代替简易装置中的长颈漏斗控制水流量
如果将盛有CuSO4溶液的试管除去,能证明生成的气体是乙炔吗
不能,乙炔中往往含有H2S、PH3等杂质,也能与酸性高