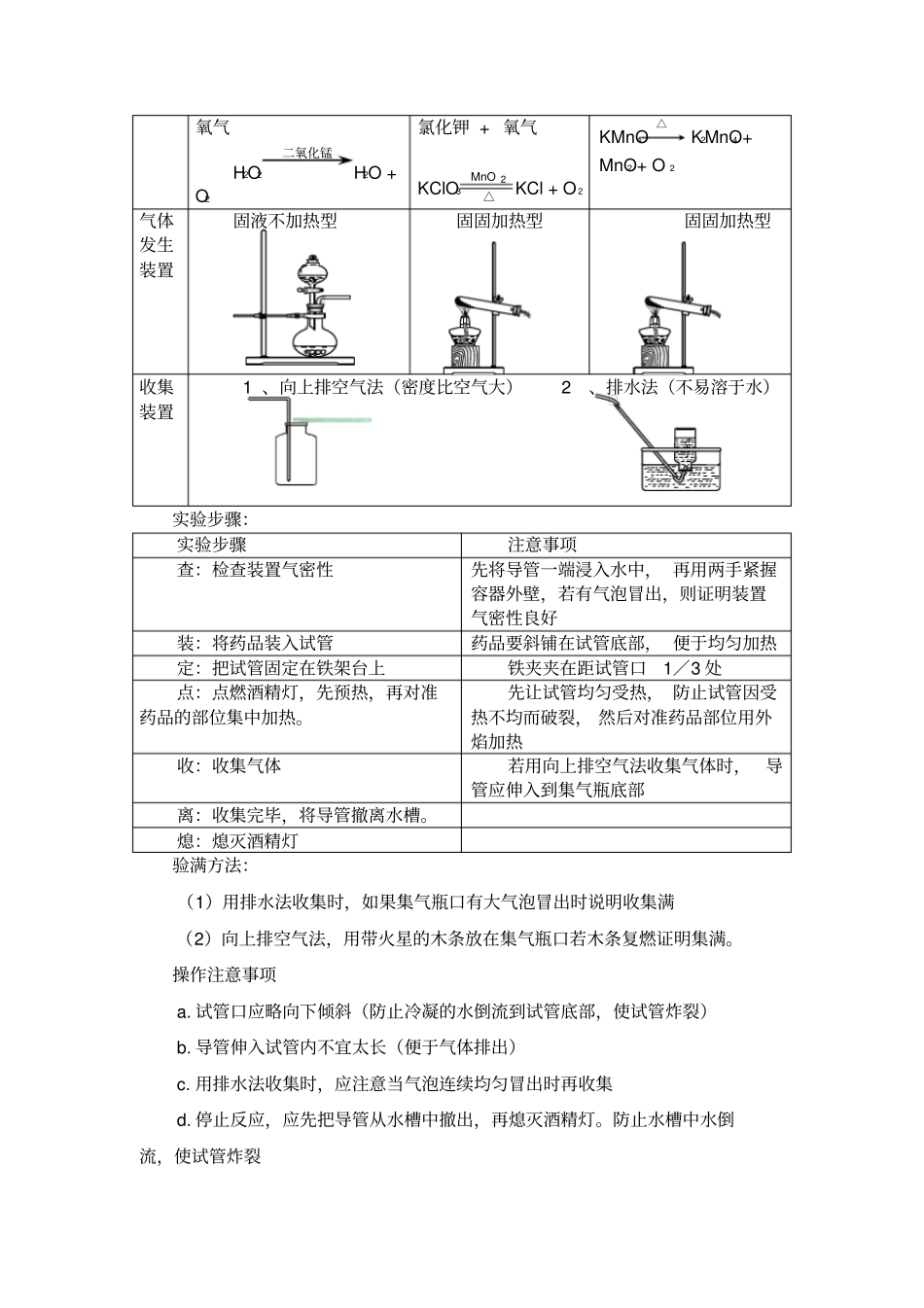
制取氧气【教学目标】:1、了解实验室制取氧气的反应原理、实验装置、实验操作
2、了解实验室中制取气体的思路和方法
【师生共同探究,总结】:药品选择1、无毒无害没有污染(环保)2、装置简便易于操作(简便)3、易于反应常温更好(安全)4、节约能源价格便宜(成本)排空气法收集:(如图1)①收集密度比空气大的气体(如:O2或CO2),气体从b端进,空气从a端出
②收集密度比空气小的气体(如:H2),气体从a端进,空气从b端出
③若用水将瓶中的气体排出,水龙头应接b导管,气体从a端出
(水的密度大于空气)2、排水法收集:(如图2)瓶中盛满水
气体从a端进,水从b端出总结:用洗气瓶排空气收集气体的连接:密小则短进长出,密大则长进短出;用洗气瓶排水收集气体的连接:短进长出
收集氧气可以用排水法的原因是(氧气不易溶于水也不与水反应)2
集满氧气瓶用玻璃片盖好后,瓶口应向(上)放置,原因是(氧气密度比空气大,处于空气下方(瓶口朝下会导致氧气逸出气体不纯))3
用排空法收集满氧气后,应先(撤除导管),后(熄灭酒精灯),其原因是(先熄灭酒精灯会导致试管变冷试管内压强减小导致液体倒吸,使试管破裂)4
若用向上排空法收集满氧气后,应先(验满)后(停止收集)其原因是(没什么原因,就是看看满了没有)怎样记忆制取氧气七步骤
答:可以用要点记忆法,每项只记一个字
即查(检查装置的气密性)、装(装入药品)、定(固定在铁架台上)、点(点燃酒精灯加热)、收(等气泡均匀连续出现时收集气体)、移(实验完毕先从水槽中移出导气管)、熄(最后熄灭酒精灯)
查、装、定、点、收、移、熄,这话听起来像“茶庄定点收利息”,用谐音记忆法,比较容易记住
氧气的工业制法————-分离液态空气法工业上需要的大量氧气采用分离液态空气法,先把空气变成液态,然后控温蒸发,得到氮气和氧气特点:量大,设备要求高,成本高氧气的实验室制法过氧化氢+二氧