液体燃烧热的测定——乙醇、本地菜籽油及调和油燃烧热的测定——文玉成、袁文龙实验原理:燃烧热:1mol物质完全燃烧时所放出的热量
恒容条件下测得的燃烧热称为恒容燃烧热QV,QV=ΔU
恒压条件下测得的燃烧热为恒压燃烧热Qp,Qp=ΔH
若把参加反应的气体和生成的气体作为理想气体处理,则存在如下关系式:------------------(1)其中:Δn为反应产物中气体物质的总摩尔数与反应物中气体物质总摩尔数之差;R为气体常数;T为反应前后绝对温度
本实验采用氧弹式量热计测量乙醇、本地菜籽油及调和油的燃烧热
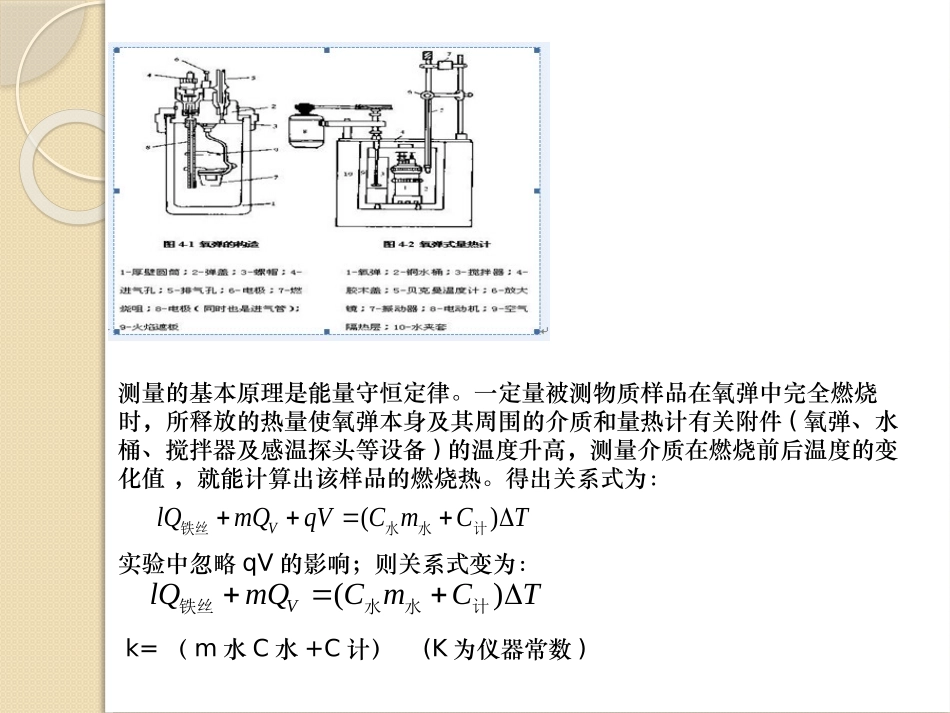
氧弹是一具特制的不锈钢容器,如图4-1所示
为保证样品在其中迅速而完全地燃烧,需要用过量的强氧化剂,通常氧弹中充以氧气作为氧化剂
实验时氧弹是旋转在装有一定量水的不锈钢桶中,水桶外是空气隔热层,再外面是恒定的水夹套,如图4-2所示
()pVQQRTng测量的基本原理是能量守恒定律
一定量被测物质样品在氧弹中完全燃烧时,所释放的热量使氧弹本身及其周围的介质和量热计有关附件(氧弹、水桶、搅拌器及感温探头等设备)的温度升高,测量介质在燃烧前后温度的变化值,就能计算出该样品的燃烧热
得出关系式为:实验中忽略qV的影响;则关系式变为:k=(m水C水+C计)(K为仪器常数)()VlQmQqVCmCT计铁丝水水()VlQmQCmCT计铁丝水水式中:QV——样品的恒容燃烧热(J·g-1);m样品——样品的质量(g);C计——量热计热容,它包括氧弹、量热计及水的热容(J·K-1);ΔT——准确温差(K);Q铁丝——点火丝燃烧热
铁丝为-6696
4J·g-1、镍丝为-3158
9J·g-1、Cu-Ni丝为-3136
2J·g-1
要测量样品的QV必须先知量热计的热容C计,测定的方法是用一定量已知燃烧热的标准物质(常用苯甲酸,QV=—26477J·