高中化学期末复习第一章物质结构元素周期律章末阶段复习必备学案新人教版必修2【知识网络构建】对所学知识及时总结,将其构建成知识网络,既有助于整体把握知识结构,又利于加深对知识间内在联系的理解
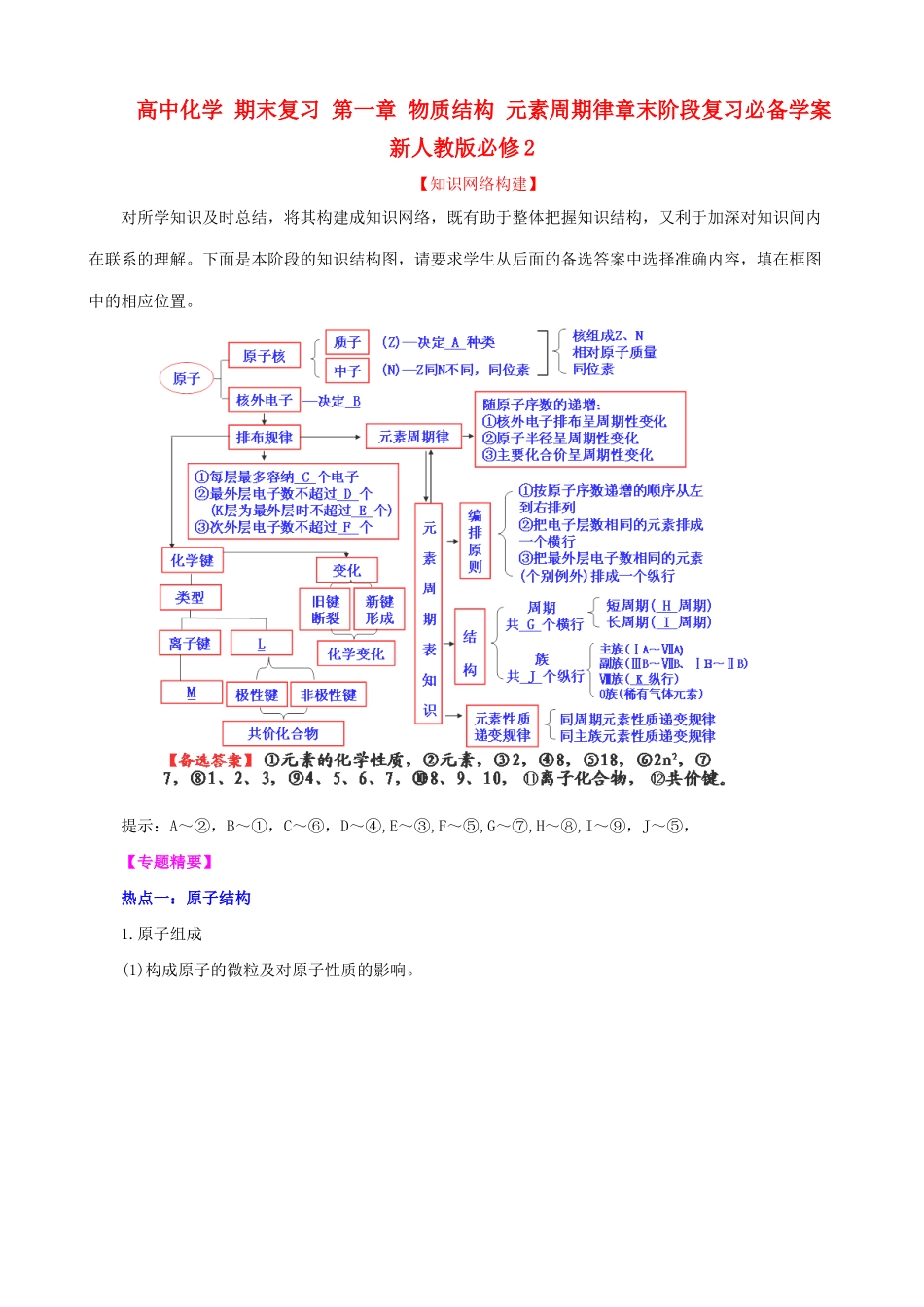
下面是本阶段的知识结构图,请要求学生从后面的备选答案中选择准确内容,填在框图中的相应位置
提示:A~②,B~①,C~⑥,D~④,E~③,F~⑤,G~⑦,H~⑧,I~⑨,J~⑤,【专题精要】热点一:原子结构1
原子组成(1)构成原子的微粒及对原子性质的影响
(2)原子中三种微粒的三种关系
①数量关系质子数(Z)=核电荷数=核外电子总数②质量关系质量数(A)=质子数(Z)+中子数(N)③电性关系a
原子:核电荷数=核外电子总数b
离子:阳离子的核外电子数=质子数-电荷数阴离子的核外电子数=质子数+电荷数2
原子核外电子排布(1)核外电子排布规律
①核外电子总是尽先排布在能量最低的电子层里
②各电子层最多容纳的电子数目是2n2
③最外层电子数不超过8个(K层为最外层时不超过2个)
④次外层电子数不超过18个,倒数第三层电子数不超过32个
(2)部分短周期元素核外电子排布的特殊性
短周期元素核外电子排布的特殊性是解答元素推断题的突破口
如:原子核中无中子的原子是H;最外层电子数是次外层电子数2倍的元素是C;最外层电子数是次外层电子数3倍的元素是O;最外层电子数是次外层电子数4倍的元素是Ne等
3.元素、核素、同位素的关系(1)核素的“两同两不同”:同元素、同质子数;不同中子数、不同原子
(2)同种元素,可以有若干种不同的核素
(3)同位素是同一元素的不同核素之间的互相称谓,不指具体的原子
【训练1】(2012·绵阳高一检测)已知R2+核外有a个电子,b个中子
表示R原子符号正确的是()A.B.C.D.【解析】选C
R元素的质子数为a+2,再由“质子数+中子数=质量数”可得质量数为a+b+2,故C