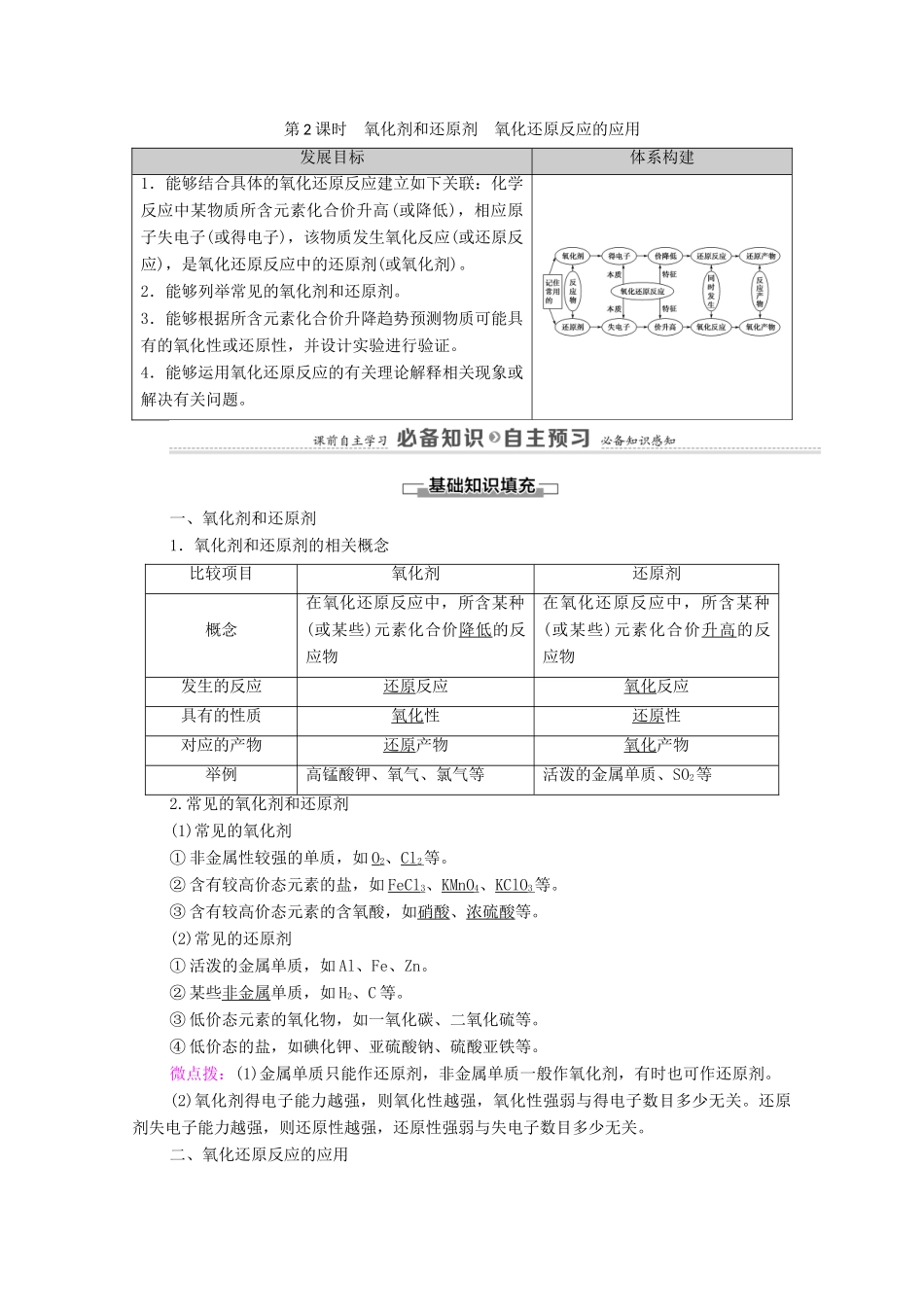
第2课时氧化剂和还原剂氧化还原反应的应用发展目标体系构建1.能够结合具体的氧化还原反应建立如下关联:化学反应中某物质所含元素化合价升高(或降低),相应原子失电子(或得电子),该物质发生氧化反应(或还原反应),是氧化还原反应中的还原剂(或氧化剂)
2.能够列举常见的氧化剂和还原剂
3.能够根据所含元素化合价升降趋势预测物质可能具有的氧化性或还原性,并设计实验进行验证
4.能够运用氧化还原反应的有关理论解释相关现象或解决有关问题
一、氧化剂和还原剂1.氧化剂和还原剂的相关概念比较项目氧化剂还原剂概念在氧化还原反应中,所含某种(或某些)元素化合价降低的反应物在氧化还原反应中,所含某种(或某些)元素化合价升高的反应物发生的反应还原反应氧化反应具有的性质氧化性还原性对应的产物还原产物氧化产物举例高锰酸钾、氧气、氯气等活泼的金属单质、SO2等2
常见的氧化剂和还原剂(1)常见的氧化剂①非金属性较强的单质,如O2、Cl2等
②含有较高价态元素的盐,如FeCl3、KMnO4、KClO3等
③含有较高价态元素的含氧酸,如硝酸、浓硫酸等
(2)常见的还原剂①活泼的金属单质,如Al、Fe、Zn
②某些非金属单质,如H2、C等
③低价态元素的氧化物,如一氧化碳、二氧化硫等
④低价态的盐,如碘化钾、亚硫酸钠、硫酸亚铁等
微点拨:(1)金属单质只能作还原剂,非金属单质一般作氧化剂,有时也可作还原剂
(2)氧化剂得电子能力越强,则氧化性越强,氧化性强弱与得电子数目多少无关
还原剂失电子能力越强,则还原性越强,还原性强弱与失电子数目多少无关
二、氧化还原反应的应用1.研究物质的性质(1)氧化性、还原性与价态的关系元素处于最低价态时,只有还原性;元素处于中间价态时既有氧化性又有还原性,但一般情况下主要表现某一方面的性质;元素处于最高价态时,只有氧化性
(2)H2O2的氧化性和还原性探究①预测H2O2中的氧元